Поражение легких при скв: Легочные проявления системных аутоиммунных заболеваний | #07/14
Легочные проявления системных аутоиммунных заболеваний | #07/14
В основе поражения легких (ПЛ) при системных аутоиммунных заболеваниях (САЗ) лежат расстройства механизмов иммунорегуляции и гиперреактивность организма. Макрофаги и лимфоциты являются ключевыми клетками, участвующими в инициации и сохранении иммунного ответа в легких. Альвеолярные макрофаги — резиденты легочной ткани — поглощают чужеродные агенты, проникшие через слизистые поверхности легких и бронхов. Кроме того, эти клетки служат в качестве антигенпредставляющих клеток для Т-лимфоцитов. Относительно небольшое число лимфоцитов присутствуют в нормальной паренхиме легких. Однако после стимуляции соответствующим антигеном окружающей лимфоидной ткани лимфоциты мигрируют в легкие и принимают участие в воспалительной реакции.
По существу, все САЗ оказываются зависимыми от неадекватной активации аутореактивных CD4+ Т-клеток и В-клеток.
Проведение специальных исследований, включавших компьютерную томографию высокого разрешения (КТВР) и биопсию легкого, выявило, что при САЗ встречаются различные гистологические формы поражения интерстиция легких (табл.).
Системная красная волчанка
Системная красная волчанка (СКВ) — системное аутоиммунное заболевание неизвестной этиологии, характеризующееся гиперпродукцией органоспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов.
С точки зрения гистологии СКВ характеризуется определенной комбинацией воспаления и фиброза, а клинический фенотип диктуется относительным «вкладом» каждого пораженного органа. Поражение тканей, по-видимому, опосредовано характерной выработкой аутоантител, формированием иммунных комплексов и их органоспецифическим отложением.

Ревматоидный артрит
Ревматоидный артрит (РА) — системное аутоиммунное заболевание соединительной ткани с преимущественным поражением суставов по типу хронического прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями.
ПЛ при РА было впервые описано в 1948 г., когда Эллман и Болл установили диффузный фиброз легких у трех пациентов. Легочные проявления при РА включают поражение плевры, образование ревматоидных узелков в легких, ИПЛ, легочный васкулит, альвеолярные кровоизлияния, бронхообструктивные изменения. Почти у половины больных РА при вскрытии выявляется плеврит. Экссудативный плеврит может быть односторонним или двусторонним и сохраняться в течение многих месяцев. Наличие плеврального выпота вызывает нарушение легочной функции. Как правило, плевральная жидкость бывает экссудативной с низким содержанием глюкозы и низким уровнем комплемента.
Ревматоидные узелки (РУ), как единичные, так и множественные, могут быть обнаружены в легочной паренхиме больных РА. РУ легких у пациентов с РА были впервые описаны Каплан в 1953 г. РУ могут появиться до, во время или после начала РА. ИПЛ характеризуется хроническим воспалением стенок альвеол и скоплением больших мононуклеарных клеток в альвеолах. Довольно часто у больных РА встречается сочетание ИПЛ и подкожных ревматоидных узелков. Прогноз для пациентов с РА с ИПЛ неблагоприятен. Легочный васкулит является одним из редких легочных проявлений РА. Альвеолярные кровоизлияния, не часто встречающиеся у больных РА, приводят к кровохарканью и анемии. У пациентов с РА отмечается высокая частота поражения бронхов. ПЛ может быть результатом токсического воздействия препаратов, используемых в терапии РА. Для того чтобы обеспечить оптимальный эффект от лечения, врач всегда должен учитывать возможную легочную патологию при оценке состояния пациентов с РА [1–3].
Системная склеродермия
Системная склеродермия (ССД) — диффузное заболевание соединительной ткани с прогрессирующим фиброзом, распространенными вазоспастическими нарушениями и характерными изменениями кожи, опорно-двигательного аппарата и внутренних органов. Среди висцеральных проявлений ССД ПЛ занимает важное место.
Плеврит при ССД наблюдается реже, чем при РА и СКВ. В то же время у больных ССД значительно выше частота ИПЛ, при этом морфологическое исследование показывает выраженный фиброз интерстициальной ткани и утолщение межальвеолярных перегородок. Исследование функции внешнего дыхания (ФВД) демонстрирует снижение диффузионной способности легких (ДСЛ) даже при отсутствии каких-либо клинических симптомов и рентгенологических изменений.
У пациентов с ССД выявляется рестриктивный тип нарушения вентиляции легких. У большинства больных ССД с ЛФ наблюдается гистологическая картина обычной интерстициальной пневмонии (ОИП), однако во многих случаях встречается гистопатологический тип неспецифической интерстициальной пневмонии (НИП).
Развитие ЛФ инициируется микрососудистыми изменениями, которые приводят к повреждению эндотелиальных клеток и поражению альвеолярного эпителия. Это приводит к активации каскада свертывания (рис.).
Экспрессия аутоантител является предиктором поражения внутренних органов, в частности ПЛ. Наличие антител к Scl-70 (антисклеродермальные антитела с молекулярной массой 70 кДа, антитела к топоизомеразе I) в значительной степени является фактором риска развития ИПЛ, в то время как антицентромерные антитела (АЦА) говорят о низкой вероятности развития рентгенологических признаков ЛФ.
У пациентов с ССД встречается легочная гипертензия (ЛГ). ЛГ может быть изолированной, возникшей вследствие поражения сосудов, или вторичной — при поражении паренхимы легких или левых отделов сердца. ЛГ развивается у 5–7% больных, чаще на поздних стадиях лимитированной формы ССД. Предиктор ЛГ — изолированное уменьшение ДСЛ. Более редко встречаются аспирационная пневмония, причиной которой является дисфункция пищевода, а также спонтанный пневмоторакс, лекарственный пневмонит [1–3, 6–8].
Полимиозит/дерматомиозит
Полимиозит/дерматомиозит (ПМ/ДМ) — группа хронических диффузных заболеваний поперечнополосатой мускулатуры, основным проявлением которых выступает мышечная слабость.
Около 40% пациентов с ПМ/ДМ имеют патологию легочной системы. Одной из причин этого является поражение мышц. Поражение межреберных мышц и высокое стояние диафрагмы приводят к уменьшению экскурсии грудной клетки и появлению вентиляционных нарушений по рестриктивному типу. В отличие от других САЗ, ПЛ при ПМ/ДМ не затрагивает в первую очередь дыхательные пути или плевру. Наиболее распространенной патологией является аспирационная пневмония, которая возникает по причине слабости мышц глотки и верхней трети пищевода.
Поражение интерстиция легких затрагивает преимущественно нижние отделы. ИПЛ может иметь медленнопрогрессирующее или фульминантное течение. Важным прогностическим фактором является наличие антител к аминоацилсинтетазам транспортной РНК (тРНК), чаще всего (антител к гистидил-тРНК-синтетазе (анти-Jo-1)). Тестирование анти-Jo-1 помогает в диагностике ПМ/ДМ с антисинтетазным синдромом, который характеризуется острым началом миозита, ИПЛ, лихорадкой, артритом, феноменом Рейно и изменением кожи кистей по типу «рука механика». Реже у больных ПМ/ДМ встречаются облитерирующий бронхиолит с организующей пневмонией и диффузное поражение альвеол [1–3, 9–11].
Тестирование анти-Jo-1 помогает в диагностике ПМ/ДМ с антисинтетазным синдромом, который характеризуется острым началом миозита, ИПЛ, лихорадкой, артритом, феноменом Рейно и изменением кожи кистей по типу «рука механика». Реже у больных ПМ/ДМ встречаются облитерирующий бронхиолит с организующей пневмонией и диффузное поражение альвеол [1–3, 9–11].
Болезнь Шегрена
Болезнь Шегрена (БШ) — системное аутоиммунное заболевание неизвестной этиологии, характеризуется поражением секретирующих эпителиальных желез, с вовлечением преимущественно слюнных и слезных желез (ксеростомия, ксерофтальмия).
Поражение экзокринных желез верхних дыхательных путей часто приводит к сухости носовых ходов и бронхов. Наиболее распространенным проявлением ПЛ, связанным с БШ, является лимфоцитарный пневмонит, поражающий нижние доли. У пациентов с БШ может развиться плеврит (с или без выпота), ИПЛ с очагами лимфоидной инфильтрации. При развитии неходжкинских лимфом метастатические поражения легких встречаются часто, реже наблюдают формирование MALT-ткани (mucosal-associated lymphoid tissue) с развитием первичной MALT-лимфомы [1–3, 12, 13].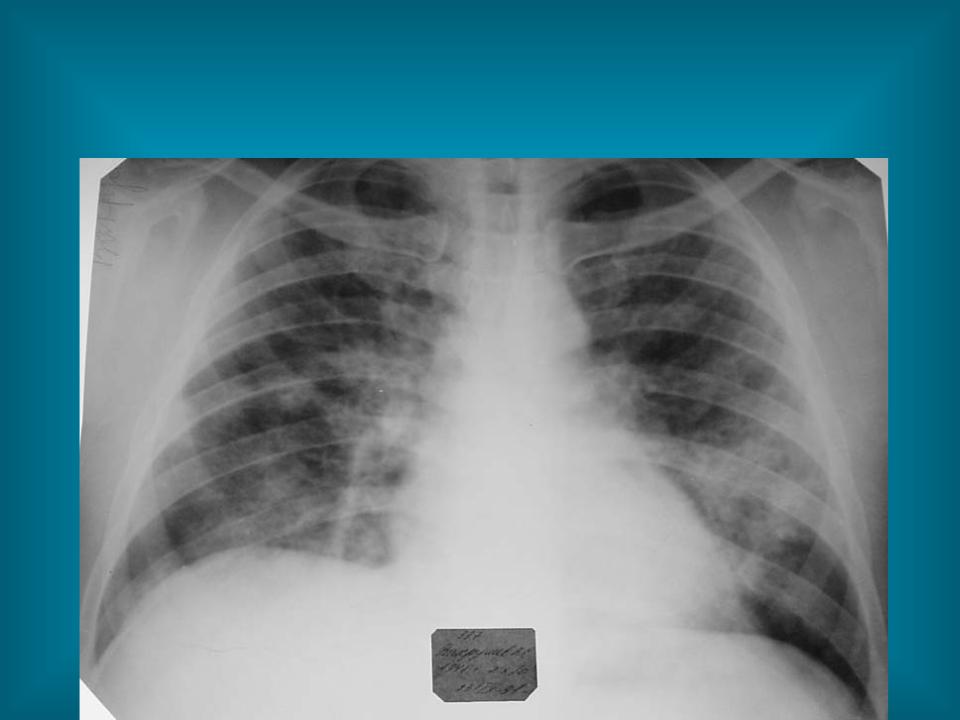
Смешанное заболевание соединительной ткани
Смешанное заболевание соединительной ткани (синдром Шарпа) (CЗСТ) — аутоиммунное заболевание, характеризующееся наличием отдельных признаков СКВ, ССД, РА, ПМ/ДМ в сочетании с высоким титром антител к экстрагируемому ядерному антигену — U1-RNP.
ИПЛ и ЛГ довольно часто встречаются у больных с СЗСТ, при этом нередко имеют субклиническое течение. Обследование пациентов с СЗСТ показало повышение уровня иммунных комплексов (ИК) и увеличение потребления комплемента. ИК-опосредованное повреждение альвеолярно-капиллярной мембраны и легочной ткани может играть важную роль в патогенезе ИПЛ при СЗСТ. При исследовании показателей функции внешнего дыхания больные с СЗСТ демонстрируют снижение диффузионной способности легких (ДСЛ) и рестриктивный тип нарушения вентиляции. Прогноз ИПЛ у пациентов с СЗСТ более благоприятный, чем при РА и ССД. ЛГ является основной причиной смерти больных с СЗСТ [1–3, 14, 15].
Гранулематоз Вегенера
Гранулематоз Вегенера (ГВ) — системный некротический васкулит мелких вен и артерий с образованием гранулем в сосудистых стенках и окружающих тканях дыхательных путей, почек и других органов.
ПЛ развивается у большинства пациентов с ГВ. Клинические проявления ПЛ при ГВ разнообразны, начиная от бессимптомных узелков в легких и кончая фульминантным альвеолярным кровотечением. ГВ может сопровождаться образованием опухолевидных инфильтратов с неровными краями, которые могут распадаться и образовывать полости. Плеврит, легочное кровотечение и увеличение лимфатических узлов средостения встречаются редко. Поражение трахеальных или бронхиальных стенок обычно проявляется гранулематозным утолщением слизистой оболочки или подслизистого слоя, при этом возникает обструктивный тип нарушения вентиляции легких. Частое осложнение — коллапс бронхов и постобструктивная пневмония. Инфильтраты, которые могут увеличиваться и уменьшаться, первоначально часто неправильно диагностируются как пневмония. Примерно в 20% случаев развивается прогрессирующая легочная недостаточность, связанная с ЛФ, пневмонией или пневмонитом, индуцированным циклофосфамидом. ДСЛ, как правило, уменьшена, но при развитии диффузных альвеолярных геморрагий наблюдают ее рост. Описаны случаи развития бронхоплевральных свищей [1–3].
Описаны случаи развития бронхоплевральных свищей [1–3].
Синдром Чарджа–Стросса
Синдром Чарджа–Строса (СЧС) — эозинофильное, гранулематозное воспаление респираторного тракта и некротизирующий васкулит, поражающий мелкие и средние сосуды, часто сочетающийся с астмой и эозинофилией.
Легкие — это наиболее поражаемый орган при данном синдроме; более 90% пациентов с синдромом СЧС в анамнезе имеют астму. При рентгенологическом исследовании легких выявляются очаги консолидации, распределяющиеся по периферии, которые часто бывают преходящими. Могут появляться узелки, при распаде не образующие полости. Другие менее распространенные проявления ПЛ включают утолщение междольковой перегородки и утолщение бронхиальной стенки. Плевральные выпоты образуются редко.
Существуют три фазы развития СЧС: продромальная фаза, которая характеризуется наличием аллергических заболеваний (как правило, астма или аллергический ринит), может продолжаться от нескольких месяцев до многих лет; эозинофилия/фаза инфильтрации тканей, в которой может наблюдаться удивительно высокая периферическая эозинофилия, а также инфильтрация эозинофилами тканей легких, желудочно-кишечного тракта и других органов; васкулитная фаза, в которой некротический васкулит поражает широкий спектр органов — сердце, легкие, периферические нервы и кожу. Диагноз приходится верифицировать с другими васкулитами, в первую очередь ГВ [1–3].
Диагноз приходится верифицировать с другими васкулитами, в первую очередь ГВ [1–3].
Синдром Гудпасчера
Синдром Гудпасчера (СГ) (геморрагический легочно-почечный синдром) — прогрессирующее аутоиммунное заболевание легких и почек, характеризующееся образованием антител к базальным мембранам капилляров клубочков почек и альвеол и проявляющееся сочетанием легочных и почечных геморрагий.
Патоморфологически в легких наблюдается картина венулитов, артериолитов, капилляритов с выраженными явлениями деструкции и пролиферации; поражение капилляров наблюдается преимущественно в межальвеолярных перегородках, развивается альвеолит с геморрагическим экссудатом в альвеолах.
В большинстве случаев ПЛ и почек происходит одновременно. Клинические проявления ПЛ включают в себя кашель, одышку и кровохарканье, которое может появляться на несколько месяцев раньше признаков поражения почек. В развитии альвеолита при СГ огромное значение имеет активация альвеолярных макрофагов. В активированном состоянии они выделяют около 40 цитокинов. Цитокины I группы (хемотаксины, лейкотриены, интерлейкин-8) усиливают поступление полиморфноядерных лейкоцитов в легкие. Цитокины II группы (факторы роста — тромбоцитарный, макрофагальный) способствуют перемещению в легкие фибробластов. Альвеолярные макрофаги продуцируют также активные формы кислорода, протеазы, повреждающие легочную ткань.
В активированном состоянии они выделяют около 40 цитокинов. Цитокины I группы (хемотаксины, лейкотриены, интерлейкин-8) усиливают поступление полиморфноядерных лейкоцитов в легкие. Цитокины II группы (факторы роста — тромбоцитарный, макрофагальный) способствуют перемещению в легкие фибробластов. Альвеолярные макрофаги продуцируют также активные формы кислорода, протеазы, повреждающие легочную ткань.
Исследование жидкости бронхоальвеолярного лаважа (ЖБАЛ) не является диагностическим при СГ, но может использоваться для подтверждения наличия диффузной альвеолярной геморрагии у пациентов с гломерулонефритом и легочными инфильтратами, но без кровохарканья. ЖБАЛ, которая остается геморрагической после многократных промываний, позволяет подтвердить диффузный геморрагический синдром, особенно при сопутствующем снижении гематокрита.
Гистологическое и иммунологическое исследование биоптатов легочной ткани при СГ характеризуется признаками геморрагического альвеолита, гемосидероза и интерстициального фиброза, а также линейных отложений иммуноглобулина G (IgG) и С3-компонента комплемента на базальных мембранах легочных альвеол.
Рентгено-компьютерное исследование легких при СГ демонстрирует наличие легочных инфильтратов в прикорневой области с распространением на нижние и средние отделы легких. Исследование легочных тестов выявляет рестриктивный тип нарушения вентиляции легких (снижение жизненной емкости легких — ЖЕЛ), но по мере прогрессирования заболевания присоединяются обструктивные изменения (снижение объема форсированного выдоха за 1 сек — ОФВ1, индекса Тиффно) [1–3].
Болезнь Бехтерева (анкилозирующий спондилит)
Болезнь Бехтерева (ББ, анкилозирующий спондилит, АС) — хроническое системное заболевание, характеризующееся воспалительным поражением суставов позвоночника, околопозвоночных тканей и крестцово-подвздошных сочленений с анкилозированием межпозвоночных суставов и развитием кальцификации спинальных связок.
ПЛ у больных АС встречается в 50–85% случаев и обусловлено анкилозирующим процессом в грудном отделе позвоночника, снижением дыхательной экскурсий грудной клетки, утомлением и слабостью дыхательных мышц. У больных АС чаще всего развивается эмфизема легких, затем ИПЛ, хроническая обструктивная болезнь легких (ХОБЛ), апикальный фиброз, бронхоэктазия и поражение плевры. Апикальный пневмофиброз, который встречается нечасто (3–4%), требует проведения дифференциальной диагностики с туберкулезными изменениями. Фиброз верхней доли легкого обычно протекает бессимптомно, но может вызывать кашель, отделение мокроты и одышку.
У больных АС чаще всего развивается эмфизема легких, затем ИПЛ, хроническая обструктивная болезнь легких (ХОБЛ), апикальный фиброз, бронхоэктазия и поражение плевры. Апикальный пневмофиброз, который встречается нечасто (3–4%), требует проведения дифференциальной диагностики с туберкулезными изменениями. Фиброз верхней доли легкого обычно протекает бессимптомно, но может вызывать кашель, отделение мокроты и одышку.
При АС чаще встречается рестриктивный тип нарушения вентиляции легких. У больных АС с хронической обструктивной болезнью легких (ХОБЛ) исследование ФВД демонстрирует обструктивные вентиляционные изменения [1, 16, 17].
Заключение
Таким образом, при САЗ могут наблюдаться различные типы легочной патологии. Развитие ПЛ обусловлено особенностями патофизиологических характеристик основного заболевания. Основные легочные проявления САЗ включают заболевания плевры, ИПЛ, поражение бронхиального дерева. При РА и СКВ чаще, чем при других САЗ, встречается поражение плевры. ИПЛ в настоящее время все больше признается как самое частое и серьезное проявление САЗ. ПЛ у больных с САЗ оказывает существенное негативное воздействие на качество жизни (КЖ): у больных снижаются показатели КЖ, характеризующие физический, психоэмоциональный статус и социальную активность.
ИПЛ в настоящее время все больше признается как самое частое и серьезное проявление САЗ. ПЛ у больных с САЗ оказывает существенное негативное воздействие на качество жизни (КЖ): у больных снижаются показатели КЖ, характеризующие физический, психоэмоциональный статус и социальную активность.
ПЛ при САЗ имеет большое значение в формировании облика заболевания, при этом во многом определяет его тяжесть и прогноз. Наряду с базисной терапией САЗ, ПЛ необходимо рассматривать как важную мишень для терапевтического воздействия.
Литература
- Ревматология, национальное руководство. Под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008.
- Castelino F. V., Varga J. Interstitial lung disease in connective tissue diseases: evolving concepts of pathogenesis and management // Arthritis Research & Therapy. 2010; 12: 213.
- Bouros D., Pneumatikos I., Tzouvelekis A. Pleural involvement in systemic autoimmune disorders // Respiration.
 2008; 75: 361–371.
2008; 75: 361–371. - Kriegel M. A., Van Beek C., Mostaghimi A. et al. Sterile empyematous pleural effusion in a patient with systemic lupus erythematosus: a diagnostic challenge // Lupus. 2009; 18: 581–585.
- Pego-Reigosa J. M., Medeiros D. A., Osenberg D. A. Respiratory manifestations of systemic lupus erythematosus: old and new concepts // Best Pract Res Clin Rheumatol. 2009; 23: 460–480.
- Varda J., Abraham D. Systemic sclerosis: a prototypic multisystem fibrotic disorder // J Clin Invest. 2007; 117: 557–567.
- Yanaba K., Hasegawa M., Takehara K. et al. Comparative study of serum surfactant protein-D and KL-6 concentrations in patients with systemic sclerosis as markers for monitoring the activity of pulmonary fibrosis // J Rheumatol. 2004; 31: 1112–1120.
- McNearney T. A., Revelle J. D., Fischbach M. et al. Pulmonary involvement in systemic sclerosis: associations with genetic, serologic, sociodemographic, and behavioral factors // Arthritis Rheum.
 2007; 57: 318–326.
2007; 57: 318–326. - Tillie-Leblond I., Wislez M., Valeyre D. et al. Interstitial lung disease and anti-Jo-1 antibodies: difference between acute and gradual onset // Thorax. 2008; 63: 53–59.
- Chen I. J., Jan Wu Y. J., Lin C. W. et al. Interstitial lung disease in polymyositis and dermatomyositis // Clin Rheumatol. 2009; 28: 639–646.
- Fujisawa T., Suda T., Nakamura Y. et al. Differences in clinical features and prognosis of interstitial lung diseases between polymyositis and dermatomyositis // J Rheumatol. 2005; 32: 58–64.
- Ito I., Nagai S., Kitaichi M. et al. Pulmonary manifestations of primary Sjögren’s syndrome: a clinical, radiologic, and pathologic study // Am J Respir Crit Care Med. 2005; 171: 632–638.
- Parambil J. G., Myers J. L., Lindell R. M. et al. Interstitial lung disease in primary Sjögren’s syndrome // Chest. 2006; 130: 1489–1495.
- Bodolay E.
 , Szekanecz Z., Devenyi K. et al. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. 2005; 44: 656–661.
, Szekanecz Z., Devenyi K. et al. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. 2005; 44: 656–661. - Kinder B. W., Shariat C., Collard H. R. et al. Undifferentiated connective tissue disease-associated interstitial lung disease: changes in lung function // Lung 2010; 188: 143–149
- Quismorio F. P. Jr. Pulmonary involvement in ankylosing spondylitis // Curr Opin Pulm Med. 2006; 12: 342–345.
- Lee C. C., Lee S. H., Chang I. J. et al. Spontaneous pneumothorax associated with ankylosis spondylitis // Rheumatol. 2005; 44: 1538–1541.
Д. В. Бестаев1, кандидат медицинских наук
Е. Л. Насонов, доктор медицинских наук, профессор, академик РАН
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
1 Контактная информация: davidbestaev@rambler. ru
ru
Повреждение легких при антифосфолипидном синдроме | Решетняк
1. Harris E. N., Baguley E., Asherson R. A., Hughes G. R. V. Clinical and serological features of the «antiphospholipid syndrome» (APS) [abstract]. Br. J. Rheumatol. 1987; 26: 19.
2. Harris E. N. Syndrome of the black swan. Br. J. Rheum. 1987; 26: 324—326.
3. Насонов Е. Л. Антифосфолипидный синдром. М.:Литтера; 2004.
4. Hughes G. R. V., Harris E. N., Gharavi A. E. The anticardiolipin syndrome. J. Rheumatol. 1986; 13: 486—489.
5. Asherson R. A., Cervera R. ‘Primary’, ‘secondary’ and other variants of the antiphospholipid syndrome. Lupus 1994; 3: 293—298
Lupus 1994; 3: 293—298
6. Hughes G. R. V. The antiphospholipid syndrome: ten years on. Lancet 1993; 342: 341—343.
7. Wilson W. A., Gharavi A. E., Koike T. et al. International consensus statement on preliminary classification criteria for definite antiphospholipid syndrome. Arthritis Rheum. 1999; 42: 1309—1311.
8. Piette J. C., Wechsler B., Frances C. et al. Exclusion criteria for primary antiphospholipid syndrome. J. Rheumatol. 1993; 20: 1802—1804.
9. Piette J. C., Wechsler B., Frances C., Godeau P. Systemic lupus erythematosus and antiphosphoplipid syndrome: reflection about the relevance of ARA criteria. J. Rheumatol. 1992; 19: 215—222.
10. Perez R. E., McClindon J. R., Lie S. T. Primary antiphospholipid syndrome with multiorgan arterial and venous thromboses. J. Rheumatol. 1992; 19: 1289—1292.
Perez R. E., McClindon J. R., Lie S. T. Primary antiphospholipid syndrome with multiorgan arterial and venous thromboses. J. Rheumatol. 1992; 19: 1289—1292.
11. Greisman S. G., Thayasparan R. S., Godwin T. A., Lockshin M. D. Occlusive vasculopathy in systemic lupus erythematosus. Association with anticardiolipin antibody. Arch. Intern. Med. 1991; 67: 387—395.
12. Ingram S. B., Goodnight S. H., Bennet R. M. An unusual syndrome of a devasting noniflammatory vasculopathy associated with anticardiolipin antibodies. Arthritis Rheum. 1987; 30: 1167—1171.
13. Harris E. N., Bos K. An acute disseminated coagulopathy vasculopathy associated with the antiphospholipid syndrome. Arch. Intern. Med. 1991; 151: 231—233.
14. Asherson R. A., Cervera R., deGrout P. G., et al. Catastrophic antiphospholipid syndrome: international consensus statement on classification criteria and treatment guidelines. Lupus 2003; 12: 530—534.
Asherson R. A., Cervera R., deGrout P. G., et al. Catastrophic antiphospholipid syndrome: international consensus statement on classification criteria and treatment guidelines. Lupus 2003; 12: 530—534.
15. Asherson R. A., Cervera R. The catastrophic antiphospholipid antibody syndrome: a review of pathogenesis, clinical features and treatment. IMAJ. 2000; 2: 268—273.
16. Cervera R., Garcio Carraso M., Asherson R. A. Pulmonary manifestation in the antiphospholipid syndrome. In: The antiphospholipid syndrome/ ed. Asherson R. A., Cervera R., Piette J. C., Shoenfeld Y.; N.; Y;. L.; Tokyo: PRC Press Boca Raton; 1996. 161—167.
17. Tan E. M., Cohen A. S., Fries J. F. et al. The 1982 revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 1982; 25: 1271—1277.
1982; 25: 1271—1277.
18. Александрова Е. Н., Насонов Е. Л., Ковалев В. Ю. Количественный иммуноферментный метод определения антител к кардиолипину в сыворотке крови. Клинич. ревматология 1995; 4: 35—39
19. Brandt J. T., Triplett D. A., Aving B., Scharrer I. Criteria for the diagnosis of lupus anticoagulant: An update. Thromb. Haemost. 1995; 74: 1185—1190.
20. Баркаган З. С., Момот А. П. Основы диагностики нарушений гемостаза. М.: Ньюдиамед-АО; 1999.
21. Тsutsumi A., Matsuura E., Ichikawa K., et al. Antibodies to beta2-glycoprotein I and clinical manifestations in patients with systemic lupus erythematosus. Arthritis Rheum. 1996; 39: 1466—1474
22. Balestrieri G., Tincani A., Spatola L. et al. Anti b2-glycoprotein I antibodies: a marker of antiphospholipid syndrome? Lupus 1995; 4: 122—130
Balestrieri G., Tincani A., Spatola L. et al. Anti b2-glycoprotein I antibodies: a marker of antiphospholipid syndrome? Lupus 1995; 4: 122—130
23. Le Tonqueze M., Salozhin K., Dueymes M. et al. Role of beta2-glycoprotein 1 in the antiphospholipid antibody binding to endothelial cells. Lupus 1995; 4: 179—186
24. Roubey R. A. Immunology of the antiphospholipid antibody syndrome. Arthritis Rheum. 1996; 39: 1444—1454
25. Espinosa G., Cervera R., Font J. et al. Cardiac and pulmonary manifestations in the antiphospholipid syndrome. The antiphospholipid syndrome II: autoimmune thrombosis. / ed. R. A. Asherson, R. Cervera, J-C. Piette. Y. Shoenfeld: Elsevier Science; 2002.
26. Jamieson S. W., Auger W. R., Fedulo P. F. Expierence and results with 150 pulmonary thrombectomy operations over a 29-month period. J. Thorac Cardiovasc. Surg. 1993; 106: 116—127.
W., Auger W. R., Fedulo P. F. Expierence and results with 150 pulmonary thrombectomy operations over a 29-month period. J. Thorac Cardiovasc. Surg. 1993; 106: 116—127.
27. Sandoval J., Amigo M. C., Barragan R. et al. Primary antiphospholipid syndrome presenting as chronic thromboembolic hypertension. Treatment with thromboendarterectomy. J. Rheumatol. 1996; 23: 772—775.
28. Luchi M. E., Asherson R. A., Lahita R. G. Primary idiopathic pulmonary hypertension complicated by arterial thrombosis. Association with antiphospholipid antibodies. Arthritis Rheum. 1992; 35: 700—705.
29. Dela Mata J., Comez Sanchez M. A., Aranzana M., Gomez-Reino J. J. Long-term iloprost infusion therapy for severe pulmonary hypertension in patients with connective tissue disease. Arthritis Rheum. 1994; 37: 1528—1533.
Arthritis Rheum. 1994; 37: 1528—1533.
30. Rich S., Kieras K., Hhait K. et al. Antinuclear antibodies in primary pulmonary hypertension. J. Am. Coll. Cardiol. 1986; 8: 1307—1311.
31. Rich S., Kaufman E., Levy P. S. The effect of high doses of calcium-channel blockers on survival in primary pulmonary hypertension. N. Engl. J. Med. 1992; 327: 76—81.
32. Humbert M., Sanchez O., Faroukh M. et al. Treatment of severe pulmonary hypertension secondary to connective tissue diseases with continuous IV epoprostenol (prostacyclin). Chest 1998; 114 (suppl 1): 80—82.
33. Nagawa Y., Masuda M., Shiihara H. et al. Successful pulmonary throboendartectomy for chronic thromboembolic pulmonary hypertension associated with anticardiolipin antibodies: report of case. Surg. Today 1992; 22: 548—552.
Surg. Today 1992; 22: 548—552.
34. Asherson R. A., Hackett D., Gharavi A. E. et al. Pulmonary hypertension in systemic lupus erythematosus. A report of three cases. J. Rheum. 1986; 12: 416—420.
35. Yokoi T., Tomita Y., Fukaya M. et al. Pulmonary hypertension associated with SLE: predominantly thrombotic arteriopathy accompanied by plexiform lesions. Arch. Pathol. Lab. Med. 1998; 122: 467—470.
36. Brucato A., Baudo F., Barberis M. et al. Pulmonary hypertension secondary to thrombosis of the pulmonary vessels in a patients with the primary antiphospholipid syndrome. J. Rheumatol. 1994; 21: 942—944.
37. Maggiorini M., Knoblauch A., Schneider J. et al. Diffuse microvascular pulmonary thrombosis associated with primary antiphospholipid antibody syndrome. Eur. Respir. J. 1997; 10: 727—730.
Eur. Respir. J. 1997; 10: 727—730.
38. Gertner E., Lie J. T. Pulmonary capillaritis, alveolar hemorrhage, and recurrent microvascular thrombosis in primary antiphospholipid syndrome. J. Rheumatol. 1993; 20: 1224—1228.
39. Adonopoulos A. P. Adult respiratory distress syndrome: An unrecognized premortem event in systemic lupus erythematosus. Br. J. Rheumatol. 1991; 30: 346—348.
40. Asherson R. A., Cervera R., Piette J. C., et al. Catastrophic antiphospholipid syndrome: clues to the pathogenesis from a series of 80 patients. Medicine (Baltimore) 2001; 80: 355—376.
41. Ingram S. B., Goodnight S. H., Bennet R. M. An unusual syndrome of a devasting, noniflammatory vasculopathy associated with anticardiolipin antibodies. Arthritis Rheum. 1987; 30: 1167—1171.
Arthritis Rheum. 1987; 30: 1167—1171.
42. Ghosh S., Walters H. D., Joist J. H. et al. Adult respiratory distress syndrome associated with antiphospholipid antibody syndrome. J. Rheumtol. 1993; 20: 1406—1408.
43. Shwab E. P., Shumacher R. Ir., Freundlich B., Callegari P. E. Pulmonary alveolar hemorrhage in systemic lupus erythematosus. Semin. Arthritis Rheum. 1993; 23: 8—15.
44. Gertner E. Diffuse alveolar hemorrhage in the antiphospholipid syndrome: spectrum of the disease and treatment. J. Rheumatol. 1999; 26: 805—807.
45. Branch D. W., Kochenour N. K., Rok N. S., Scott J. R. A new postpartum syndrome associated with antiphospholipid antibodies. In: Proceedings of the II International Symposium on Antiphospholipid Antibodies. 1986. 3—10.
1986. 3—10.
46. Решетняк Т. М., Александрова Е. Н., Штивельбанд И. Б. и др. Катастрофический антифосфолипидный синдром: диагностика и терапия. Терапевт. арх. 2005; 5: 18—21.
Врачи ревматологического отделения больницы №4 спасли пациентку с тяжёлым течением системной красной волчанки
Молодую москвичку привезли в одну из московских больниц с подозрением на пневмонию. Состояние пациентки было тяжелым, на консультацию к ней пригласили ревматолога городской клинической больницы №4 Департамента здравоохранения Москвы Екатерину Ильину. Врач диагностировала системную красную волчанку — одно из сложнейших аутоиммунных заболеваний. Для дальнейшего лечения женщину перевели в ревматологическое отделение городской больницы №4 (Павловской больницы).
Системная красная волчанка, которую в народе называют «болезнью с тысячью лиц» – это заболевание, при котором в организме появляются антитела к собственной ДНК. Из-за этого болезнь затрагивает практически весь организм: могут повреждаться любые клетки и ткани, и возникает системное воспаление. Чаще всего страдают соединительные ткани, почки и сердечно-сосудистая система.
Из-за этого болезнь затрагивает практически весь организм: могут повреждаться любые клетки и ткани, и возникает системное воспаление. Чаще всего страдают соединительные ткани, почки и сердечно-сосудистая система.
У пациентки болезнь приняла самое неблагоприятное течение и имела высокую степень активности. В процесс были вовлечены практически все органы и системы, поражена кожа, легкие, почки, суставы, печень, развился полисерозит – воспаление нескольких серозных оболочек сразу (плевры, перикарда, брюшины). Кроме того перечень диагнозов дополнял миокардит, васкулит, лихорадка, лимфаденопатия, гепатоспленомегалия, гематологические и иммунологические нарушения.
Пациентке назначили пульстерапию метилпреднизолоном. Так называют введение больших доз лекарств прерывистым способом для усиления их терапевтического воздействия и уменьшения побочных эффектов. А затем перевели её на обычное применение этого препарата.
На фоне проводимой терапии была достигнута положительная динамика: у женщины улучшилось самочувствие, результаты анализов стали приходить в норму. Однако болезнь не собиралась отступать и нанесла новый удар. Теперь к имеющимся проблемам пациентки присоединилась двухсторонняя пневмония.
Однако болезнь не собиралась отступать и нанесла новый удар. Теперь к имеющимся проблемам пациентки присоединилась двухсторонняя пневмония.
Почти две недели за жизнь пациентки боролись в отделении реанимации. С учетом тяжелых добавившихся диагнозов, к которым впоследствии присоединился также абсцесс левого легкого с прорывом в плевральную полость, лечение требовало точной и индивидуальной корректировки доз препаратов, чередования их комбинаций. А также коллегиального подхода: в спасении пациентки принимали участие ревматологи, анестезиологи-реаниматологи, пульмонологи, торакальные хирурги.
Благодаря слаженной работе команды врачей, угроза жизни Зои вскоре миновала, а потом стало улучшаться самочувствие, и женщина пошла на поправку.
Сейчас пациентка находится под наблюдением специалистов, принимает необходимые препараты. Её состояние доктора оценивают как стабильное, а недавнее обследование показало: данных за активность системной красной волчанки в организме Зои нет.
| Соискатель: | Лейнеман Яна Андреевна |
| Тип диссертации: | Диссертация на соискание ученой степени кандидата медицинских наук |
| Название работы: | Клинические варианты поражений легких при системной красной волчанке (дифференциальная диагностика и принципы лечения) |
| Дата защиты диссертации: | 20 декабря 2016 г. |
| Шифр научной специальности: | 14.01.04 — Внутренние болезни |
| Отрасль науки: | Медицинские науки |
| Диссертационный совет: | Д 215. 002.06 002.06 |
| Название организации: | Федеральное государственное бюджетное военное образовательное учреждение высшего образования «Военно-медицинская академия имени С.М. Кирова» Министерства обороны Российской Федерации |
| Адрес организации: | 194044, Санкт — Петербург, ул. Академика Лебедева, д. 6 |
| Телефон: | 8(812)292-32-06 |
| Е-mail: | [email protected] |
| Опубликовано: | 16 сентября 2016 г. |
Публикации в СМИ
Волчанка — род заболеваний, протекающих с поражением кожи. Термин волчанка (lupus) ранее применяли для описания эрозий кожи (напоминают волчьи укусы). В отечественной литературе различают волчанку обыкновенную (l. vulgaris, волчанка туберкулёзная), волчанку красную (l. erythematosus) и волчанку ознобленную (l. pernio) с дальнейшим подразделением.
Термин волчанка (lupus) ранее применяли для описания эрозий кожи (напоминают волчьи укусы). В отечественной литературе различают волчанку обыкновенную (l. vulgaris, волчанка туберкулёзная), волчанку красную (l. erythematosus) и волчанку ознобленную (l. pernio) с дальнейшим подразделением.
Волчанка красная
Заболевание из группы коллагенозов, характеризующееся поражением суставов, серозных оболочек, кожи, внутренних органов, ЦНС; в патогенезе определяющую роль играет образование аутоантител, в т.ч. к ДНК. Выделяют красную волчанку с преимущественным поражением кожи и доброкачественным течением (дискоидная волчанка красная, дискоидная волчанка) и генерализованную форму (СКВ, системная волчанка).
• Волчанка красная бородавчатая (волчанка красная вегетирующая) характеризуется появлением на поражённых участках кожи бородавчатых разрастаний • Волчанка красная буллёзная характеризуется появлением на поражённых участках кожи мелких пузырей • Волчанка красная геморрагическая характеризуется кровоизлияниями в поражённые участки кожи • Волчанка красная гипертрофическая — форма дискоидной красной волчанки, характеризующаяся наличием резко выступающих над поверхностью кожи участков • Волчанка красная глубокая (волчанка красная гиподермическая, Капоши–Ирганга глубокая волчанка красная) — форма дискоидной красной волчанки, характеризующаяся ограниченным, обычно одиночным очагом с распространяющимся в дерму воспалительным инфильтратом • Волчанка красная дискоидная (волчанка красная хроническая, себорея конгестивная, эритема атрофическая, эритематоз) — волчанка красная с преобладанием поражения кожи в виде эритемы, гиперкератоза и атрофии, как правило, локализующихся на лице в форме бабочки; является самостоятельным заболеванием • Волчанка красная диссеминированная (l. erythematosus disseminatus) — волчанка, характеризующаяся множественными эритематозно-отёчными или папулёзными высыпаниями, локализующимися преимущественно на открытых участках кожи • Волчанка красная мутилирующая характеризуется рубцеванием очагов поражения, что приводит к деформации носа и ушных раковин • Волчанка красная опухолевидная — вариант гипертрофической красной волчанки с формированием очага кожного поражения в виде красно-фиолетовой бляшки, напоминающей опухоль • Волчанка красная пигментная — форма дискоидной красной волчанки, отличающаяся тёмно-коричневой окраской поражённых участков кожи • Волчанка красная поверхностная (Биетта центробежная эритема) — волчанка, характеризующаяся появлением на лице и других открытых участках кожи резко ограниченной интенсивной эритемы, увеличивающейся по периферии, без выраженного гиперкератоза и атрофии; возможны поражение внутренних органов и переход в СКВ • Волчанка красная подострая характеризуется выраженным дерматитом, обусловленным фотосенсибилизацией.
erythematosus disseminatus) — волчанка, характеризующаяся множественными эритематозно-отёчными или папулёзными высыпаниями, локализующимися преимущественно на открытых участках кожи • Волчанка красная мутилирующая характеризуется рубцеванием очагов поражения, что приводит к деформации носа и ушных раковин • Волчанка красная опухолевидная — вариант гипертрофической красной волчанки с формированием очага кожного поражения в виде красно-фиолетовой бляшки, напоминающей опухоль • Волчанка красная пигментная — форма дискоидной красной волчанки, отличающаяся тёмно-коричневой окраской поражённых участков кожи • Волчанка красная поверхностная (Биетта центробежная эритема) — волчанка, характеризующаяся появлением на лице и других открытых участках кожи резко ограниченной интенсивной эритемы, увеличивающейся по периферии, без выраженного гиперкератоза и атрофии; возможны поражение внутренних органов и переход в СКВ • Волчанка красная подострая характеризуется выраженным дерматитом, обусловленным фотосенсибилизацией. Чаще возникает у мужчин. Характерны полиартрит, серозит; обнаруживают АТ к протеину, входящему в состав РНК (La-Аг). Поражений почек и ЦНС не наблюдают • Волчанка красная роговая — красная волчанка, характеризующаяся образованием на поверхности поражённых участков кожи очагов гиперкератоза, напоминающих кожный рог • Волчанка красная себорейная — форма дискоидной красной волчанки, сходная с себорейной экземой по характеру эритемы и шелушения • Волчанка красная системная (СКВ) — воспалительное заболевание соединительной ткани с разнообразными проявлениями: лихорадкой, болями в суставах или артритами, диффузными эритематозными поражениями кожи лица, шеи, верхних конечностей с дегенерацией по типу разжижения базального слоя эпидермиса и его атрофией, лимфаденопатией, плевритом, перикардитом, гломерулонефритом, анемией, наличием широкого спектра аутоантител • Волчанка красная телеангиэктатическая — форма дискоидной красной волчанки, характеризующаяся образованием на поражённых участках кожи большого количества телеангиэктазий • Волчанка красная туберкулоидная — форма дискоидной красной волчанки, характеризующаяся сходством по виду поражённых участков кожи с обыкновенной волчанкой • Волчанка красная хроническая — см.
Чаще возникает у мужчин. Характерны полиартрит, серозит; обнаруживают АТ к протеину, входящему в состав РНК (La-Аг). Поражений почек и ЦНС не наблюдают • Волчанка красная роговая — красная волчанка, характеризующаяся образованием на поверхности поражённых участков кожи очагов гиперкератоза, напоминающих кожный рог • Волчанка красная себорейная — форма дискоидной красной волчанки, сходная с себорейной экземой по характеру эритемы и шелушения • Волчанка красная системная (СКВ) — воспалительное заболевание соединительной ткани с разнообразными проявлениями: лихорадкой, болями в суставах или артритами, диффузными эритематозными поражениями кожи лица, шеи, верхних конечностей с дегенерацией по типу разжижения базального слоя эпидермиса и его атрофией, лимфаденопатией, плевритом, перикардитом, гломерулонефритом, анемией, наличием широкого спектра аутоантител • Волчанка красная телеангиэктатическая — форма дискоидной красной волчанки, характеризующаяся образованием на поражённых участках кожи большого количества телеангиэктазий • Волчанка красная туберкулоидная — форма дискоидной красной волчанки, характеризующаяся сходством по виду поражённых участков кожи с обыкновенной волчанкой • Волчанка красная хроническая — см. Волчанка дискоидная красная.
Волчанка дискоидная красная.
Волчанка обыкновенная
Волчанка обыкновенная (волчанка, волчанка туберкулёзная, туберкулёз кожи люпозный) — форма туберкулёза кожи, характеризующаяся образованием люпом, сливающихся в сплошные очаги и приводящих к атрофии кожи; локализуется преимущественно на лице; возможно поражение слизистых оболочек • Волчанка обыкновенная веррукозная — форма обыкновенной волчанки, отличающаяся образованием бородавчатых разрастаний на поверхности поражённых участков • Волчанка обыкновенная гипертрофическая — форма обыкновенной волчанки, отличающаяся резким выступанием поражённых участков над поверхностью кожи • Волчанка обыкновенная диссеминированная — форма обыкновенной волчанки, отличающаяся наличием множественных рассеянных мелких очагов на коже лица, туловища и конечностей • Волчанка обыкновенная диссеминированная милиарная лица (туберкулёз кожи лица милиарный диссеминированный, волчанка фолликулярная диссеминированная Фокса) — форма обыкновенной волчанки, характеризующаяся образованием на коже лица несливающихся мягких полушаровидных милиарных узелков красновато-коричневатого цвета; характерны феномен «яблочного желе» и положительная проба зондом Поспелова; возникает при гематогенной диссеминации возбудителя • Волчанка обыкновенная диффузная отличается наличием обширных сливных очагов • Волчанка обыкновенная импетигинозная — форма обыкновенной волчанки, отличающаяся образованием на поверхности поражённых участков изменений, напоминающих импетиго • Волчанка обыкновенная крустозная — форма обыкновенной волчанки, отличающаяся образованием на поверхности поражённых участков обильных корок, напоминающих кожный рог • Волчанка обыкновенная мутилирующая — форма обыкновенной волчанки, отличающаяся поражением не только кожи, но и подлежащих тканей (подкожной клетчатки, хряща, кости) и приводящая вследствие этого к обезображиванию лица • Волчанка обыкновенная опухолевидная — форма обыкновенной волчанки, характеризующаяся поражением кожи с образованием очагов, напоминающих по внешнему виду опухоль • Волчанка обыкновенная островоспалительная инфильтративная — форма обыкновенной волчанки, отличающаяся образованием на поражённых участках (чаще на коже носа) цианотично-красного массивного инфильтрата • Волчанка обыкновенная плоская — форма обыкновенной волчанки, отличающаяся незначительным выступанием поражённых участков над поверхностью кожи • Волчанка обыкновенная псориазиформная сходна с псориазом по виду поражённых участков кожи • Волчанка обыкновенная серпигинозная отличается выраженной тенденцией к периферическому распространению очагов • Волчанка обыкновенная сквамозная отличается выраженным шелушением поражённых участков кожи • Волчанка обыкновенная склеротическая отличается резким разрастанием соединительной ткани в поражённых участках кожи с формированием грубого гипертрофического рубца • Волчанка обыкновенная эксфолиативная — вариант сквамозной обыкновенной волчанки, характеризующаяся образованием на поверхности поражённых участков крупных, легко отторгающихся чешуек • Волчанка обыкновенная эритематозная клинически сходна с дискоидной красной волчанкой • Волчанка обыкновенная язвенная отличается изъязвлением поражённых участков кожи.
Волчанка ознобленная
Волчанка ознобленная (ознобленная волчанка Бенье–Теннессона, ознобленная гранулёма Цилера) — клинический вариант саркоидоза, характеризующийся наличием на коже фиолетовых плотных выпуклых пятен с выявляемыми при диаскопии желтоватыми включениями • Волчанка ознобленная Хатчинсона (chilblain lupus) — заболевание, характеризующееся наличием признаков красной волчанки и папулонекротического туберкулёза кожи, протекающее в виде синевато-красных очагов поражения на лице.
Сопутствующие термины
• Волчаночноклеточный феномен (LE-феномен, Харгрейвса феномен) — наблюдаемый при СКВ фагоцитоз лейкоцитами клеточных ядер, разрушенных АНАТ, с формированием клеток красной волчанки • Фактор волчаночный — АНАТ • Клетки красной волчанки (LE-клетки, Харгрейвса клетки) — зрелые нейтрофильные гранулоциты со смещёнными к периферии ядрами вследствие фагоцитоза ядерного вещества другой клетки; при окраске эозином имеют вид гомогенных шаров розового цвета; обнаруживаются в периферической крови больных СКВ • Люпома — первичный морфологический элемент высыпаний при обыкновенной волчанке в виде крупного бугорка коричневато-красного цвета тестовидной консистенции (скопление мелких туберкулёзных бугорков).
Волчанка отдельных органов и систем
• Гепатит волчаночный (люпоидный) — устаревший термин для обозначения варианта хронического активного гепатита с многообразием внепечёночных проявлений, при котором обнаруживаются АНАТ • Эндокардит Либмана (синдром Капоши–Либмана–Сакса, эндокардит Либмана–Сакса) — острый абактериальный бородавчатый эндокардит при СКВ • Люпус-артрит (артрит волчаночный, полиартрит волчаночный) — полиартрит при СКВ • Люпус-нефрит (нефрит волчаночный) — поражение ткани почки при СКВ в виде утолщения базальной мембраны клубочков, отложения фибрина, наличия гиалиновых тромбов и гематоксилиновых телец, феномена «проволочной петли» • Люпус-пневмонит (пневмонит волчаночный) — поражение лёгких при СКВ, протекающее по типу васкулита • Нейролюпус — общее название поражений нервной системы при СКВ.
Близкие термины и состояния • Livedo (livedo reticularis) — древовидный рисунок на коже нижних конечностей (вследствие тромбоза мелких кожных сосудов), иногда сочетающийся с отёками и изъязвлениями; возникает преимущественно у женщин • Синдром Джейнуэя — наследственная агаммаглобулинемия, клинически проявляющаяся симптомами ревматоидного артрита или красной волчанки.
МКБ-10 • A18.4 Туберкулёз кожи и подкожной клетчатки • L93 Красная волчанка • M32 Системная красная волчанка
Системная красная волчанка | Общероссийская общественная организация «Ассоциация ревматологов России»
Профессор д.м.н. Татьяна Магомедалиевна Решетняк
Институт ревматологии РАМН, Москва
Эта лекция предназначена как для пациентов с системной красной волчанкой (СКВ), так и для их родственников, друзей и вообще для тех, кто хочет лучше понять это заболевание, чтобы помочь больным СКВ справиться с этим недугом. В ней изложены сведения о СКВ с разъяснениями некоторых медицинских терминов. Приведенная информация дает представление о заболевании и его симптомах, содержит сведения о диагностике и лечении, а также текущие научные достижения в этой проблеме. В лекции также обсуждаются такие вопросы, как забота о здоровье, беременности, качество жизни больных с СКВ. Если у вас будут вопросы после прочтения этой брошюры, вы можете обсудить их со своим лечащим врачом или задать вопросы по электронной почте: reshetnyak@irramn..png) ru.
ru.
Краткая история СКВ
Название красная волчанка, в латинском варианте как Lupus erythematosus, происходит от латинского слова «люпус», что в переводе на английский « wolf» означает волк и «эритематозус» — красная. Такое название было дано заболеванию из-за того, что кожные проявления были схожи с повреждениями при укусе голодным волком. Врачам этот недуг известен с 1828г, после описания французским дерматологом Biett кожных признаков. Спустя 45 лет после первого описания еще один врач дерматолог Kaposhi заметил, что некоторые больные с кожными признаками заболевания имеют еще и симптомы заболевания внутренних органов. И в 1890г. известный английский врач Osler обнаружил, что красная волчанка, называемая также системной, может протекать (хотя и редко) без кожных проявлений. В 1948г. был описан феномен LE-(ЛЕ)клеток, который характеризовался обнаружением в крови осколков клеток. Это открытие позволило врачам идентифицировать многих больных с СКВ. Только в 1954г. были выявлены в крови больных СКВ определенные белки (или антитела), которые действовали против собственных клеток. Обнаружение этих белков было использовано для разработки более чувствительных тестов для диагностики СКВ.
были выявлены в крови больных СКВ определенные белки (или антитела), которые действовали против собственных клеток. Обнаружение этих белков было использовано для разработки более чувствительных тестов для диагностики СКВ.
Что такое СКВ
Системная красная волчанка, также иногда называемая «волчанка» или коротко СКВ – тип нарушений иммунной системы, известный как аутоиммунное заболевание. При аутоиммунных заболеваниях организм, вырабатывая чужеродные белки к собственным клеткам и их компонентам, наносит ущерб своим здоровым клеткам и тканям. Аутоиммунное заболевание — это состояние, при котором иммунная система начинает воспринимать «свои» ткани как чужеродные и атакует их. Это ведет к воспалению и повреждению различных тканей организма. Волчанка – хроническое аутоиммунное заболевание, которое проявляется в нескольких формах и может вызывать воспаление суставов, мышц и различных других частей организма. Следуя из вышесказанного определения СКВ, понятно, что при этом заболевании поражаются различные органы организма, включая суставы, кожу, почки, сердце, легкие, кровеносные сосуды и мозг. Хотя у людей с этим заболеванием много различных симптомов, некоторые наиболее общие включают чрезмерную утомляемость, болезненные или опухшие суставы (артриты), необъяснимую лихорадку, кожные высыпания и проблемы с почками. СКВ относится к группе ревматических заболеваний. Ревматические заболевания включают те, сопровождающиеся воспалительным заболеванием соединительной ткани и характеризующиеся болями в суставах, мышцах, костях.
Хотя у людей с этим заболеванием много различных симптомов, некоторые наиболее общие включают чрезмерную утомляемость, болезненные или опухшие суставы (артриты), необъяснимую лихорадку, кожные высыпания и проблемы с почками. СКВ относится к группе ревматических заболеваний. Ревматические заболевания включают те, сопровождающиеся воспалительным заболеванием соединительной ткани и характеризующиеся болями в суставах, мышцах, костях.
В настоящее время, СКВ относится к неизлечимым заболеваниям. Однако симптомы СКВ могут контролироваться соответствующим лечением, и большинство людей с этим заболеванием могут вести активную, здоровую жизнь. Почти у всех больных СКВ активность ее изменяется на протяжении заболевания, чередуясь моментами, называемыми вспышками – обострениями (в англоязычной литературе именуемые как пожар) и периодами хорошего самочувствия или ремиссии. Обострение заболевания характеризуется появлением или ухудшением воспаления различных органов. По принятой в России классификации активность заболевания делится на три стадии: I-я – минимальная, II-я – умеренная и III-я – выраженная. Кроме того, по началу возникновения признаков заболевания в нашей стране различают варианты течения СКВ– острое, подоострое и первично-хроническое. Такое разделение удобно при длительном наблюдении за больными. Ремиссия заболевания – состояние, при котором нет признаков или симптомов СКВ. Случаи полной или длительной ремиссии СКВ хотя и редки, но имеют место. Понимание как предотвратить обострение и как лечить их, когда они отмечаются, помогает больным с СКВ поддерживать свое здоровье. В нашей стране – в Институте ревматологии РАМН, так же как и в других мировых научных центрах, продолжаются интенсивные исследования по достижению огромных успехов в понимании болезни, которые могут привести к излечению.
Кроме того, по началу возникновения признаков заболевания в нашей стране различают варианты течения СКВ– острое, подоострое и первично-хроническое. Такое разделение удобно при длительном наблюдении за больными. Ремиссия заболевания – состояние, при котором нет признаков или симптомов СКВ. Случаи полной или длительной ремиссии СКВ хотя и редки, но имеют место. Понимание как предотвратить обострение и как лечить их, когда они отмечаются, помогает больным с СКВ поддерживать свое здоровье. В нашей стране – в Институте ревматологии РАМН, так же как и в других мировых научных центрах, продолжаются интенсивные исследования по достижению огромных успехов в понимании болезни, которые могут привести к излечению.
Существуют два вопроса, изучаемые исследователями: кто заболевает СКВ и почему. Мы знаем, что женщины чаще, чем мужчины болеют СКВ и это соотношение по данным различных научных центров колеблется от 1:9 до 1:11. По данным американских исследователей СКВ в три раза чаще поражает чернокожих женщин по сравнению с белой расой, а также более распространена у женщин испанского, азиатского и коренного американского происхождения. К тому же, известны семейные случаи заболевания СКВ, но риск, что ребенок или брат или сестра пациента тоже заболеют СКВ до сих пор довольно низок. Нет в Росси статистических сведений о численности больных СКВ, так как симптомы заболевания варьируют в широких пределах от минимальных до тяжелых поражений жизненно-важных органов и начало их появления часто трудно указать точно.
К тому же, известны семейные случаи заболевания СКВ, но риск, что ребенок или брат или сестра пациента тоже заболеют СКВ до сих пор довольно низок. Нет в Росси статистических сведений о численности больных СКВ, так как симптомы заболевания варьируют в широких пределах от минимальных до тяжелых поражений жизненно-важных органов и начало их появления часто трудно указать точно.
На самом деле существует несколько видов СКВ:
системная красная волчанка, которая является формой заболевания, которую большинство людей имеют в виду, когда они говорят «волчанка» или в англоязычной литературе «люпус». Слово «системная» значит, что заболевание может поражать многие системы организма. Симптомы СКВ могут быть легкими или тяжелыми. Хотя СКВ в первую очередь поражает людей в возрасте от 15 до 45 лет, она может обнаружиться как в детстве, так и в пожилом возрасте. Эта брошюра акцентирует внимание на СКВ.
дискоидная красная волчанка преимущественно поражает кожу. Красная поднимающаяся сыпь может появиться на лице, коже черепа, или где-нибудь еще. Поднимающиеся области могут становиться толстыми и чешуйчатыми. Сыпь может продолжаться днями и годами или может рецидивировать (проходить и потом вновь появляться). Небольшой процент людей с дискоидной красной волчанкой позже развивают СКВ.
Поднимающиеся области могут становиться толстыми и чешуйчатыми. Сыпь может продолжаться днями и годами или может рецидивировать (проходить и потом вновь появляться). Небольшой процент людей с дискоидной красной волчанкой позже развивают СКВ.
лекарственно индуцированная красная волчанка относится к форме волчанки, вызываемой лекарствами. Они вызывает некоторые симптомы похожие на подобные при СКВ (артрит, сыпь, лихорадка и боли в груди, но как правило не вовлекаются в процесс почки), которые исчезают при прекращении приема лекарств. Медикаменты, которые могут вызвать лекарственно индуцированную красную волчанку, включают: гидралазин (Аресолин), прокаинамид (Прокан, Пронестил), метилдопа (алдомет), гуинидин (Гуинаглют), изониазид и некоторые противосудорожные средства такие, как фенитоин (дилантин) или карбамазепин (Тегретол) и др..
неонатальная волчанка. Может поражать некоторых новорожденных, у женщин с СКВ или с определенными другими нарушениями иммунной системы. Дети с неонатальной волчанкой могут иметь тяжелые поражения сердца, которое является наиболее грозным симптомом. Некоторые новорожденныее могут иметь кожную сыпь, аномалии печени или цитопению (низкое количество клеток крови). В настоящее время врачи могут определять большинство больных с риском развития неонатальной СКВ, что позволяет быстро начинать лечение ребенка с рождения. Неонатальная волчанка встречается очень редко, и большинство детей, матери которых болеют СКВ, полностью здоровы. Следует отметить, что кожные высыпания при неонатальной волчанки обычно не требуют терапии и проходят самостоятельно.
Некоторые новорожденныее могут иметь кожную сыпь, аномалии печени или цитопению (низкое количество клеток крови). В настоящее время врачи могут определять большинство больных с риском развития неонатальной СКВ, что позволяет быстро начинать лечение ребенка с рождения. Неонатальная волчанка встречается очень редко, и большинство детей, матери которых болеют СКВ, полностью здоровы. Следует отметить, что кожные высыпания при неонатальной волчанки обычно не требуют терапии и проходят самостоятельно.
Что вызывает системную красную волчанку?
Системная красная волчанка – сложное заболевание, причина которого не известна. Вероятно, что это не одна причина, а скорее комбинация нескольких факторов, среди которых генетические, факторы окружающей среды и, возможно, гормональные, сочетание которых может вызвать заболевание. Точная причина заболевания может отличаться у разных людей, провоцирующим фактором могут быть и стресс, и простудное заболевание, и гормональная перестройка организма, которая имеет место во время полового созревания, беременности, после аборта, во время менопаузы. Ученые достигли большого прогресса в понимании некоторых возникновения ряда симптомов СКВ, которые описаны в этой брошюре. Исследователи полагают, что генетика играет важную роль в развитии заболевания, однако, специфический «ген волчанки» до сих пор не определен. Вместо этого, появилось мнение, что несколько генов могут увеличить восприимчивость человека к этой болезни.
Ученые достигли большого прогресса в понимании некоторых возникновения ряда симптомов СКВ, которые описаны в этой брошюре. Исследователи полагают, что генетика играет важную роль в развитии заболевания, однако, специфический «ген волчанки» до сих пор не определен. Вместо этого, появилось мнение, что несколько генов могут увеличить восприимчивость человека к этой болезни.
Факт, что волчанка может протекать в семьях, показывает, что развитие заболевания имеет генетическую основу. К тому же, изучение однояйцевых близнецов показало, что волчанка с большей вероятностью приведет к поражению обоих близнецов, у которых одинаковый набор генов, чем двоих разнояйцевых близнецов или других детей одних родителей. Так как риск заболеть для однояйцевых близнецов много меньше чем 100 процентов, поэтому ученые думают, что одни гены не могут объяснять факт возникновения волчанки. Другие факторы также должны играть роль. Среди них, которые интенсивно продолжают изучаться, включают солнечное излучение, стресс, определенные лекарства и инфекционные агенты, такие, как вирусы. В тоже время СКВ не является инфекционным или контагиознымзаболеванием, не относится к онкологическим заболеваниям и синдрому приобритенного иммунодефицита. Хотя вирус и может вызывать заболевание у восприимчивых к нему людей, человек не может «поймать» волчанку от какого-либо другого больного.
В тоже время СКВ не является инфекционным или контагиознымзаболеванием, не относится к онкологическим заболеваниям и синдрому приобритенного иммунодефицита. Хотя вирус и может вызывать заболевание у восприимчивых к нему людей, человек не может «поймать» волчанку от какого-либо другого больного.
При СКВ иммунная система организма не работает так, как должна. Здоровая иммунная система продуцирует антитела, которые являются специфическими протеинами – белками, которые помогают бороться и разрушать вирусы, бактерии и другие чужеродные вещества, вторгающиеся в организм. При волчанке иммунная система продуцирует антитела (белки) против здоровых клеток и тканей собственного организма. Эти антитела, называемые аутоантителами («ауто» значит свои, собственные) способствуют воспалению различных частей организма, вызывая их опухание, покраснение, повышение температуры и боль. К тому же, некоторые аутоантитела соединяются с субстанциями из собственных клеток и тканей организма для формирования молекул, называемых иммунными комплексами. Образование этих иммунных комплексов в организме также способствует воспалению и повреждению тканей у больных волчанкой. Ученые еще не поняли все факторы, которые вызывают воспаление и повреждение тканей при волчанке и это является активной областью исследования.
Образование этих иммунных комплексов в организме также способствует воспалению и повреждению тканей у больных волчанкой. Ученые еще не поняли все факторы, которые вызывают воспаление и повреждение тканей при волчанке и это является активной областью исследования.
Симптомы СКВ.
Несмотря на наличие определенных признаков заболевания, каждый случай больного СКВ различен. Клинические проявления СКВ могут колебаться от минимальных до тяжелых поражений жизненно-важных органов и могут периодически появляться и уходить. Общие симптомы волчанки приведены в таблице и включают повышенную утомляемость (синдром хронической усталости), болезненность и припухлость суставов, необъяснимую лихорадку и кожные высыпания. Характерная кожная сыпь может появиться на переносице и на щеках и из-за того, что по форме напоминает бабочку называется «бабочкой» или эритематозная (красная) сыпь на коже скуловой области. Высыпания красного цвета могут появиться на любой части кожи тела: на лице или ушах, на руках – плечах и кистях, на коже груди.
Общие симптомы СКВ
- Болезненность и припухание суставов, мышечная боль
- Необъяснимая лихорадка
- Синдром хронической усталости
- Высыпания на коже лица красного цвета или смена окраски кожиных покровов
- Боли в грудной клетке при глубоком дыхании
- Усиленное выпадение волос
- Побеление или посинение кожи пальцев кистей или стоп на холоде или при стрессе (синдром Рейно)
- Повышенная чувствительность к солнцу
- Припухание (отеки) ног и/или вокруг глаз
- Увеличение лимфатических узлов
Другие симптомы волчанки включают боль в груди, выпадение волос, чувствительность к солнцу, анемию (уменьшению красных клеток крови), и бледность или багровость кожи пальцев рук или ног от холода и стресса. Некоторые люди также испытывают головные боли, головокружение, депрессию или судороги. Новые симптомы могут продолжать появляться спустя годы после постановки диагноза, также как и различные признаки болезни могут проявиться в различное время.
У некоторых больных СКВ вовлекается только одна какая-либо система организма, например кожа или суставы, или органы кроветворения. У других больных проявления заболевания могут затрагивать многие органы и заболевание носит полиорганный характер. Тяжесть поражения систем организма различна у разных больных. Более часто поражаются суставы или мышцы, вызывая артриты или боль в мышцах — миалгии. Кожные высыпания довольно схожи у разных пациентов. При полиорганном проявлении СКВ следующие системы организма могут быть вовлечены в патологический процесс :
почки: воспаление в почках (волчаночный нефрит) может ухудшать их функциональную способность, которая сводится к эффективному выведению ненужных продуктов и токсинов из организма. Так как функциональная способность почек очень важна для общего здоровья, поражение их при волчанке, как правило, требует интенсивного медикаментозного лечения, чтобы предотвратить необратимые повреждения. Самому больному обычно трудно оценить степень поражения почек, так обычно воспаление почек при СКВ (волчаночном нефрите) не сопровождается болью, ассоциированной с вовлечением в процесс почек, хотя некоторые больные могут заметить, что их лодыжки опухли, появилась припухлость вокруг глаз. Часто показателем поражения почек при волчанке является ненормальный анализ мочи и уменьшение количества мочи.
Часто показателем поражения почек при волчанке является ненормальный анализ мочи и уменьшение количества мочи.
центральная нервная система: у некоторых пациентов волчанка поражает мозг или центральную нервную систему. Это может вызывать головные боли, головокружение, нарушения памяти, проблемы со зрением, параличи или изменения в поведении (психозы), судороги. Некоторые из этих симптомов, однако, могут быть вызваны некоторыми лекарственными препаратами, в том числе и применяемыми для лечения СКВ или эмоциональным стрессом от знакомства с этим заболеванием.
кровеносные сосуды: кровеносные сосуды могут воспаляться (васкулиты), поражая путь, по которому кровь циркулирует в организме. Воспаление может быть слабым и не требовать лечения.
кровь: у больных волчанкой может развиться анемия или лейкопения (уменьшение числа белых и/или красных кровяных клеток). Волчанка также может вызвать тромбоцитопению — уменьшение числа тромбоцитов в крови, которое ведет к увеличению риска кровотечения. Некоторые пациенты с волчанкой имеют повышенный риск образования тромбов в кровеносных сосудах.
Некоторые пациенты с волчанкой имеют повышенный риск образования тромбов в кровеносных сосудах.
сердце: у некоторых людей с волчанкой воспаление может быть в артериях, которые приносят кровь к сердцу (коронарный васкулит), самом сердце (миокардит или эндокардит) или в серозной оболочке, которая окружает сердце (перикардит), вызывая боли в груди или другие симптомы.
легкие: некоторые больные СКВ развивают воспаление серозной оболочки легких (плеврит), вызывая боли в грудной клетке, одышку и кашель. Аутоиммунное воспаление легких называется пневмонитом. В воспалительный процесс могут вовлекаться другие серозные оболочки, покрывающие печень, селезенку, вызывая болезненность в соответствующем расположении данного органа.
Диагностика системной красной волчанки.
Диагностика волчанки может быть трудной. Это может занять месяцы или даже годы для врачей, чтобы собрать симптомы и точно диагностировать это сложное заболевание. Признаки, упоминаемые в этой части, больной может развивать в течение длительного периода болезни или за короткий промежуток времени. Диагностика СКВ строго индивидуальна и нельзя по наличию одного какого-либо симптома верифицировать это заболевание. Правильный диагноз волчанки требует знаний и осведомленности со стороны доктора и хорошая связь со стороны пациента. Рассказать доктору полную, точную медицинскую историю (например, какие проблемы со здоровьем у вас были и как долго, что провоцировало появление болезни) крайне необходимо для процесса диагностики. Эта информация, вместе с объективным обследованием и результатами лабораторных тестов, помогает врачу принимать во внимание другие заболевания, которые могут быть похожи на СКВ, или действительно подтвердить ее. Для постановки диагноза может потребоваться время, и болезнь может быть верифицирована не сразу, а только при появлении новых симптомов.
Диагностика СКВ строго индивидуальна и нельзя по наличию одного какого-либо симптома верифицировать это заболевание. Правильный диагноз волчанки требует знаний и осведомленности со стороны доктора и хорошая связь со стороны пациента. Рассказать доктору полную, точную медицинскую историю (например, какие проблемы со здоровьем у вас были и как долго, что провоцировало появление болезни) крайне необходимо для процесса диагностики. Эта информация, вместе с объективным обследованием и результатами лабораторных тестов, помогает врачу принимать во внимание другие заболевания, которые могут быть похожи на СКВ, или действительно подтвердить ее. Для постановки диагноза может потребоваться время, и болезнь может быть верифицирована не сразу, а только при появлении новых симптомов.
Нет одного теста, который может определить, болеет ли человек СКВ, но несколько лабораторных анализов могут помочь врачу поставить диагноз. Используют анализы, определяющие специфические аутоантитела часто присутствующие у больных волчанкой. Например, анализ на антинуклеарные антитела обычно проводится для выявления аутоантител, которые противодействуют компонентам ядра, или «командному центру» собственных клеток человека. Многие больные имеют положительный анализ на антинуклеарные антитела; однако, некоторые лекарства, инфекции и другие заболевания также могут вызвать положительный результат. Анализ на антинуклеарные антитела просто дает другой ключ для доктора делать заключение в постановке диагноза. Также есть анализы крови для индивидуальных типов аутоантител, которые более специфичны для людей с волчанкой, хотя не все люди с волчанкой имеют положительный для них результат. Эти антитела включают анти-ДНК, анти- Sm, RNP, Ro ( SSA), La ( SSB). Врач может использовать эти анализы, чтобы подтвердить диагноз волчанки.
Например, анализ на антинуклеарные антитела обычно проводится для выявления аутоантител, которые противодействуют компонентам ядра, или «командному центру» собственных клеток человека. Многие больные имеют положительный анализ на антинуклеарные антитела; однако, некоторые лекарства, инфекции и другие заболевания также могут вызвать положительный результат. Анализ на антинуклеарные антитела просто дает другой ключ для доктора делать заключение в постановке диагноза. Также есть анализы крови для индивидуальных типов аутоантител, которые более специфичны для людей с волчанкой, хотя не все люди с волчанкой имеют положительный для них результат. Эти антитела включают анти-ДНК, анти- Sm, RNP, Ro ( SSA), La ( SSB). Врач может использовать эти анализы, чтобы подтвердить диагноз волчанки.
Согласно диагностическим критериям Американской Коллегии Ревматологов, пересмотра 1982г., имеется 11 следующих признаков:
Одиннадцать диагностических признаков СКВ
- высыпания красного цвета в скуловой области (в форме «бабочки», на коже груди в зоне «декольте», на тыле кистей)
- дискоидная сыпь (чешуйчатые, дисковидной формы изъязвления чаще на коже лица, волосистой части головы или грудной клетке)
- фоточувствительность (чувствительность к солнечным лучам за короткий промежуток времени (не более 30 минут)
- язвы ртовой полости (боли в горле, на слистых ротовой полости или носа)
- артриты (болезненность, припухание, скованность в суставах)
- серозиты (воспаление серозной оболочки вокруг легких, сердца, брюшины, вызывая боль при перемене положения тела и часто сопровождающееся затруднением дыхания)_
- вовлечение почек
- проблемы, связанные с поражением центральной нервной системы (психозы и судороги, не связанные с приемом лекарств)
- гематологические проблемы (уменьшение количества клеток крови)
- иммунологические нарушения (которые увеличивают риск присоединения вторичных инфекций)
- антиядерные антитела (аутоантитела которые действуют против ядер собственных клеток организма, когда эти части клеток ошибочно воспринимаются как чужеродные (антиген)
Эти диагностические критерии разработаны, чтобы доктор мог отличить СКВ от других заболеваний соединительной ткани, причем для постановки диагноза достаточно 4 из вышеперечисленных признаков. В тоже время, наличие только одного какого-то признака не исключает болезнь. Кроме признаков, входящих в диагностические критерии, больные СКВ могут иметь дополнительные симптомы заболевания. К ним относятся трофические нарушения (снижение веса, усиленное выпадение волос до появления очагов облысения или полного облысения), лихорадку немотивированного характера. Иногда первым признаком заболевания может быть необычная смена окраски кожных покровов (посинение, побеление) пальцев или части пальца, носа, ушных раковин на холоде или эмоциональном напряжении. Подобная смена окраски кожных покровов называется синдромом Рейно. Другие общие симптомы заболевания могут иметь место – это мышечная слабость, субфебрильная температура, снижение или потеря аппетита, неприятные ощущения в животе, сопровождающиеся тошнотой, рвотой, а иногда диареей.
В тоже время, наличие только одного какого-то признака не исключает болезнь. Кроме признаков, входящих в диагностические критерии, больные СКВ могут иметь дополнительные симптомы заболевания. К ним относятся трофические нарушения (снижение веса, усиленное выпадение волос до появления очагов облысения или полного облысения), лихорадку немотивированного характера. Иногда первым признаком заболевания может быть необычная смена окраски кожных покровов (посинение, побеление) пальцев или части пальца, носа, ушных раковин на холоде или эмоциональном напряжении. Подобная смена окраски кожных покровов называется синдромом Рейно. Другие общие симптомы заболевания могут иметь место – это мышечная слабость, субфебрильная температура, снижение или потеря аппетита, неприятные ощущения в животе, сопровождающиеся тошнотой, рвотой, а иногда диареей.
Около 15% больных СКВ также имеют синдром Шегрена ( Sjogren’ s) или так называемый «сухой синдром». Это хроническое состояние, которое сопровождается сухостью глаз и полости рта. У женщин может отмечаться и сухость слизистых половых органов (влагалища).
У женщин может отмечаться и сухость слизистых половых органов (влагалища).
Иногда больные с СКВ испытывают депрессии или невозможность концентрировать внимание. Быстрая смена настроения или необычное поведение может встречаться по следующим причинам:
Эти явления могут быть связаны с аутоиммунным воспалением в центральной нервной системе
Эти проявления могут быть нормальной реакцией к изменению своего самочувствия
Состояние может быть связано с нежелательными эффектами лекарственных препаратов, особенно когда добавляется новый препарат или появляются новые симптомы ухудшения. Повторяем, что признаки СКВ могут появляться в течение длительного периода. Хотя многие больные СКВ обычно имеют несколько признаокв заболевнаия, большинство из них обычно имеют несколько проблем со своим здоровьем, которые имеют склонность периодически обостряться. Тем не менее большинство больных СКВ, на фоне терапии чувствуют себя хорошо, не имея каких-либо признаков поражения органов.
Подобные состояния со стороны центральной нервной системы могут потребовать добавления препаратов, кроме основных лекарств, для лечения СКВ, влияющих на центральную нервную систему. Вот почему иногда терапевту-ревматологу необходима помощь врачей других специальностей, в частности психиатра, невролога и т.д.
Некоторые анализы используются менее часто, но могут быть полезны, если у больного симптомы остаются неясными. Врач может назначить биопсию кожи или почек если они поражены. Обычно при постановке диагноза назначается анализ на сифилис – реакция Вассермана, так как некоторые волчаночные антитела в крови могут вызывать ложноположительную реакцию на сифилис. Положительный анализ не означает, что пациент болен сифилисом. Кроме того, все эти анализы только помогают, чтобы дать доктору ключ и информацию к постановке правильного диагноза. Врач должен сопоставить полную картину: историю заболевания, клинические симптомы и данные анализов, чтобы точно определить, есть ли у человека волчанка.
Другие лабораторные анализы используются для наблюдения за течением заболевания с момента установления диагноза. Общий анализ крови, анализ мочи, биохимический анализ крови и скорость оседания эритроцитов (СОЭ) могут дать ценную информацию. СОЭ — показатель воспаления в организме. Она диагностирует, как быстро красные клетки крови падают на дно трубочки с несворачивающейся кровью. Однако повышение СОЭ не является важным показателем для СКВ, а в комплексе с другими показателями позволяет предупредить некоторые осложнения при СКВ. Это в первую очередь касается присоединения вторичной инфекции, которая не только осложняет состояние больного, но и создает проблемы в терапии СКВ. Другой анализ показывает уровень группы протеинов в крови, называемых комплементом. У больных волчанкой часто низкий уровень комплемента, особенно в период обострения заболевания.
Диагностические правила для СКВ
- Опрос о появлении признаков заболевания (анамнез заболевания), наличии родственников с любыми заболеваниями
- Полный врачебный осмотр (от макушки до пяток)
Лабораторное обследование:
- Общий клинический анализ крови с подсчетом всех клеток крови: лейкоцитов, эритроцитов, тромбоцитов
- Общий анализ мочи
- Биохимичекий анализ крови
- Исследование общего комплемента и некоторых компонентов комплемента, которые часто выявляются в низком при высокой активности СКВ
- Исследование антинуклеарных антител – позитивные титры у большинства больных, но позитивность может быть связана и с другими причинами
- Исследование других аутоантител (антител к двуспиральной ДНК, к рибунуклеопротеиду (РНП), анти – Ro, анти- La) – один или более из этих тестов позитивны при СКВ
- Исследование реакции Вассермана – исследование крови на сифилис, которое участи больных СКВ является ложнопозитивным, а не показателем болезни сифилисом
- Биопсия кожи и/или почек
Лечение системной красной волчанки
Тактика лечения СКВ строго индивидуальна и может меняться со временем заболевания. Диагностика и лечение волчанки — часто объединенные усилия пациента и врачей, специалистов различных специальностей. Больной может обратиться к семейному доктору или терапевту, или может посетить ревматолога. Ревматолог – это доктор, который специализируется на артритах и других заболеваниях суставов, костей и мышц. Клинические иммунологи (врачи, специализирующиеся на нарушениях иммунной системы) могут также лечить пациентов с волчанкой. В процессе лечения часто помогают другие профессионалы: это могут быть медсестры, психологи, социальные работники и также врачи-специалисты такие как нефрологи (доктора, которые лечат заболевания почек), гематологи (специализируются на нарушениях крови), дерматологи (врачи, которые лечат заболевания кожи) и неврологи (доктора, специализирующиеся в нарушениях нервной системы).
Диагностика и лечение волчанки — часто объединенные усилия пациента и врачей, специалистов различных специальностей. Больной может обратиться к семейному доктору или терапевту, или может посетить ревматолога. Ревматолог – это доктор, который специализируется на артритах и других заболеваниях суставов, костей и мышц. Клинические иммунологи (врачи, специализирующиеся на нарушениях иммунной системы) могут также лечить пациентов с волчанкой. В процессе лечения часто помогают другие профессионалы: это могут быть медсестры, психологи, социальные работники и также врачи-специалисты такие как нефрологи (доктора, которые лечат заболевания почек), гематологи (специализируются на нарушениях крови), дерматологи (врачи, которые лечат заболевания кожи) и неврологи (доктора, специализирующиеся в нарушениях нервной системы).
Появляющиеся новые направления и эффективность лечения волчанки дают врачам больший выбор в подходе к лечению заболевания. Для пациента очень важно работать в тесном контакте с врачом и принимать активное участие в своем лечении.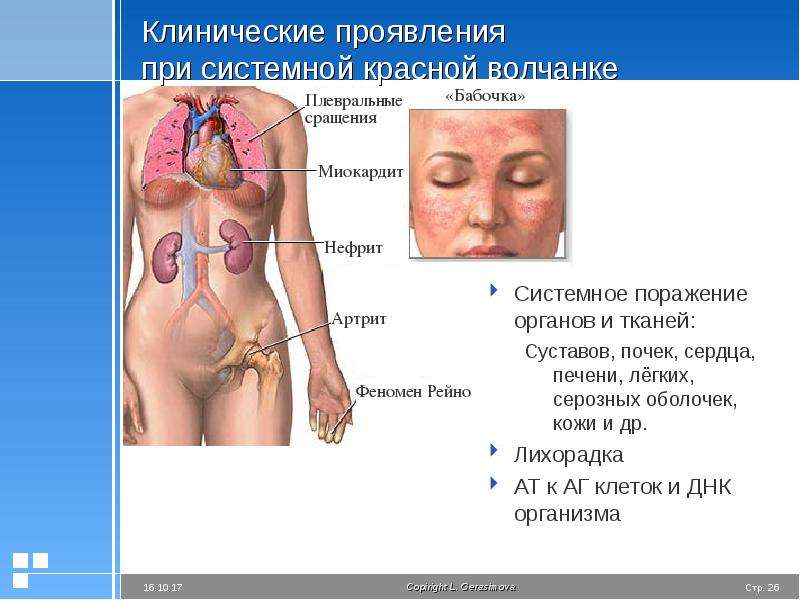 Диагностировав один раз волчанку, доктор планирует лечение, основываясь на пол, возраст пациента, состояние на момент осмотра, начало заболевания, клинические симптомы и условия жизни. Тактика лечения СКВ строго индивидуальна и может периодически меняться. Разработка плана лечения имеет несколько целей: предотвратить обострение, лечить его, когда оно имеет место, и свести к минимуму осложнения. Врач и пациент должны регулярно оценивать план лечения, чтобы убедиться, что он наиболее эффективен.
Диагностировав один раз волчанку, доктор планирует лечение, основываясь на пол, возраст пациента, состояние на момент осмотра, начало заболевания, клинические симптомы и условия жизни. Тактика лечения СКВ строго индивидуальна и может периодически меняться. Разработка плана лечения имеет несколько целей: предотвратить обострение, лечить его, когда оно имеет место, и свести к минимуму осложнения. Врач и пациент должны регулярно оценивать план лечения, чтобы убедиться, что он наиболее эффективен.
Несколько видов лекарственных препаратов используется для лечения СКВ. Доктор выбирает лечение, основываясь на симптомах и нуждах каждого пациента индивидуально. Для пациентов с болями и припуханием суставов, повышением их температуры применяют лекарства, которые уменьшают воспаление и относятся к нестероидным противовоспалительным препаратам (НПВП), они используются часто. НПВП могут использоваться одни или в комбинации с другими лекарствами, чтобы контролировать боль, припухание или повышение температуры. При покупке НПВП важно, чтобы это были указания врача, так как доза препарата для больных волчанкой может отличаться от дозы, рекомендованной на упаковке. Общие побочные эффекты НПВП, могут включать расстройства желудка, изжогу, понос и задержку жидкости в организме. Некоторые больные также отмечают развитие признаков поражения печени или почек во время приема НПВП, поэтому особенно важно для пациента оставаться в тесном контакте с врачом при лечении этими препаратами.
При покупке НПВП важно, чтобы это были указания врача, так как доза препарата для больных волчанкой может отличаться от дозы, рекомендованной на упаковке. Общие побочные эффекты НПВП, могут включать расстройства желудка, изжогу, понос и задержку жидкости в организме. Некоторые больные также отмечают развитие признаков поражения печени или почек во время приема НПВП, поэтому особенно важно для пациента оставаться в тесном контакте с врачом при лечении этими препаратами.
НЕСТЕРОИДНЫЕ ПРОТИВОВОСПАЛИТЕЛЬНЫЕ ПРЕПАРАТЫ (НПВП)
Противомалярийные препараты также используются для лечения волчанки. Эти лекарства первоначально использовались для лечения симптомов малярии, но врачи обнаружили, что они также помогают при волчанке, особенно при кожной форме. Точно не известно, как антималярийные препараты «работают» при волчанке, но ученые думают, что это происходит в результате подавления определенных этапов иммунного ответа. В настоящее время доказано, что эти препараты влияя на тромбоциты, оказывают антитромботическое действие, и еще одним положительным действием их является гиполипидемическое свойство. Специфические антималярийные средства, используемые для лечения волчанки, включают гидроксихлорохин (Плаквенил), хлорохин (Арален), хинакрин (Атабрин). Они могут использоваться отдельно или в комбинации с другими препаратами и, в основном, применяются для лечения синдрома хронической усталости, боли в суставах, кожной сыпи и поражения легких. Учеными доказано, что длительное лечение антималярийными препаратами может предотвратить рецидив заболевания. Побочные эффекты антималярийных препаратов могут включать расстройства желудка и довольно редко повреждение сетчатки глаза, органов слуха, головокружения. Появление при приеме этих препаратов светобоязни, нарушения цветоощущения требует обращения к офтальмологу. Больные СКВ, получающие антималярийные препараты, должны осматриваться окулистом не реже 1 раза в 6 месяцев при лечении плаквенилом и 1 раз в 3 месяца — при использовании делагила.
Специфические антималярийные средства, используемые для лечения волчанки, включают гидроксихлорохин (Плаквенил), хлорохин (Арален), хинакрин (Атабрин). Они могут использоваться отдельно или в комбинации с другими препаратами и, в основном, применяются для лечения синдрома хронической усталости, боли в суставах, кожной сыпи и поражения легких. Учеными доказано, что длительное лечение антималярийными препаратами может предотвратить рецидив заболевания. Побочные эффекты антималярийных препаратов могут включать расстройства желудка и довольно редко повреждение сетчатки глаза, органов слуха, головокружения. Появление при приеме этих препаратов светобоязни, нарушения цветоощущения требует обращения к офтальмологу. Больные СКВ, получающие антималярийные препараты, должны осматриваться окулистом не реже 1 раза в 6 месяцев при лечении плаквенилом и 1 раз в 3 месяца — при использовании делагила.
Основным препаратом для лечения СКВ являются препараты кортикостероидных гормонов, к которым относятся преднизолон (Делтазон), гидрокортизон, метилпреднизолон (Медрол) и дексаметазон (Декадрон, Гексадрол). Иногда в обиходе эту группу препаратов называют стероидами, но это не то же самое, что анаболические стероиды, применяемые некоторыми атлетами для накачивания мышечной массы. Эти препараты являются синтетическими формами гормонов, которые в норме продуцируются надпочечниками – железами внутренней секреции, расположенные в брюшной полости над почками. Кортикостероиды относятся к кортизолу, который является естественным противовоспалительным гормоном, быстро подавляющим воспаление. Кортизон и позже гидрокортизон – одни из первых препаратов этого семейства, применение которых в состояниях угрожающих жизни при различных заболеваниях, помогли выжить многим тысячам больным. Кортикостероиды могут быть даны в виде таблеток, кожного крема или в инъекциях. Так как это сильнодействующие лекарства, то врач будет подбирать самую низкую дозу с наибольшим эффектом. Обычно доза гормонов зависит от степени активности заболевания, а также органов вовлеченных в процесс. Поражение только почек или нервной системы уже является основанием для очень высоких доз кортикостероидов.
Иногда в обиходе эту группу препаратов называют стероидами, но это не то же самое, что анаболические стероиды, применяемые некоторыми атлетами для накачивания мышечной массы. Эти препараты являются синтетическими формами гормонов, которые в норме продуцируются надпочечниками – железами внутренней секреции, расположенные в брюшной полости над почками. Кортикостероиды относятся к кортизолу, который является естественным противовоспалительным гормоном, быстро подавляющим воспаление. Кортизон и позже гидрокортизон – одни из первых препаратов этого семейства, применение которых в состояниях угрожающих жизни при различных заболеваниях, помогли выжить многим тысячам больным. Кортикостероиды могут быть даны в виде таблеток, кожного крема или в инъекциях. Так как это сильнодействующие лекарства, то врач будет подбирать самую низкую дозу с наибольшим эффектом. Обычно доза гормонов зависит от степени активности заболевания, а также органов вовлеченных в процесс. Поражение только почек или нервной системы уже является основанием для очень высоких доз кортикостероидов. Короткосрочные (быстропроходящие) побочные эффекты кортикостероидов включают неправильное распределение жира (лунообразное лицо, отложение жировой ткани на спине по типу «горбика»), увеличение аппетита, повышение веса и эмоциональную неуравновешенность. Эти побочные эффекты в основном исчезают при снижении дозы или отмены препаратов. Но нельзя сразу прерывать прием кортикостероидов, или быстро снижать их дозу, поэтому очень важно сотрудничество врача и больного при изменении дозы кортикостероидов. Иногда врачи дают очень большую дозу кортикостероидов по вене («болюс» или «пульс» терапия). С этим лечением типичные побочные эффекты менее выражены и постепенное снижение дозы не обязателен. Важно, что бы больной вел дневник приема лекарственных препаратов, где должна быть отмечена первоначальная доза кортикостероидов, начало их снижения и темпы снижения. Это поможет доктору в оценке результатов терапии. К сожалению, на практике в последние годы часто сталкиваемся с отменой препарата даже на короткий срок в связи с отсутствием в аптечной сети препарата.
Короткосрочные (быстропроходящие) побочные эффекты кортикостероидов включают неправильное распределение жира (лунообразное лицо, отложение жировой ткани на спине по типу «горбика»), увеличение аппетита, повышение веса и эмоциональную неуравновешенность. Эти побочные эффекты в основном исчезают при снижении дозы или отмены препаратов. Но нельзя сразу прерывать прием кортикостероидов, или быстро снижать их дозу, поэтому очень важно сотрудничество врача и больного при изменении дозы кортикостероидов. Иногда врачи дают очень большую дозу кортикостероидов по вене («болюс» или «пульс» терапия). С этим лечением типичные побочные эффекты менее выражены и постепенное снижение дозы не обязателен. Важно, что бы больной вел дневник приема лекарственных препаратов, где должна быть отмечена первоначальная доза кортикостероидов, начало их снижения и темпы снижения. Это поможет доктору в оценке результатов терапии. К сожалению, на практике в последние годы часто сталкиваемся с отменой препарата даже на короткий срок в связи с отсутствием в аптечной сети препарата. Больной СКВ должен иметь кортикостероиды с запасом, с учетом выходных или праздничных дней. При отсутствии в аптечной сети преднизолон, он может быть заменен на любой другой препарат из этой группы. В таблице, приведенной ниже мы даем эквивалентные 5мг. (1 таблетке) преднизолона дозы других аналогов кортикостероидов.
Больной СКВ должен иметь кортикостероиды с запасом, с учетом выходных или праздничных дней. При отсутствии в аптечной сети преднизолон, он может быть заменен на любой другой препарат из этой группы. В таблице, приведенной ниже мы даем эквивалентные 5мг. (1 таблетке) преднизолона дозы других аналогов кортикостероидов.
Таблица. Средний эквивалентный противовоспалительный потенциал кортизона и его аналогов, основанных на размере таблеток
| Общее название (патентованное название) | Эквивалентный размер таблеток (мг) |
| Кортизона ацетат (кортон) | 25 |
| Гидрокортизон (гидрокортон) | 20 |
| Дефлазокорт (калькорт в Мексике) | 6 |
| Преднизон (делтазон) | 5 |
| Преднизолон (гиделтра) | 5 |
| Метилпреднизолон (медрол) | 4 |
| Триамсинолон (аристокорт, кеналог) | 4 |
| Параметозон | 2 |
| Флурпреднизолон | 1,5 |
| Дексаметазон (декадрон) | 0,75 |
| Бетаметазон (целестон) | 0,60 |
Несмотря на обилие дериватов кортикостероидов для длительного применения желательны преднизолон и метилпреднизолон, так как побочные эффекты других, особенно фтор-содержащих препаратов более выражены.
Длительные побочные эффекты кортикостероидов могут включать растягивающиеся рубцы – стрии на коже, чрезмерный рост волос, в связи с усиленным выведением кальция из костей последние становятся хрупкими – развивается вторичный (лекарственный) остеопроз. К нежелательным эффектам при лечении кортикостероидами относится и повышенное кровяное давление, повреждение артерий в следствие нарушения обмена холестерина, повышение сахара в крови, легко присоединяются инфекции и наконец, раннее развитие катаракты. Характерно, что чем выше доза кортикостероидов, тем тяжелее побочные эффекты. Также, чем дольше их прием, тем больше риск возникновения побочных эффектов. Ученые работают над развитием альтернативных путей, чтобы ограничить или компенсировать применение кортикостероидов. Например, кортикостероиды могут использоваться в комбинации с другими, менее сильнодействующими лекарствами, или врач может попробовать медленно уменьшать дозу после длительной стабилизации состояния. Больные волчанкой, кто принимают кортикостероиды, должны применять дополнительно кальций и витамин Д для снижения риска развития остеопороза (ослабленные, хрупкие кости).
Еще один нежелательный эффект синтетических кортикостероидов связан с развитием уменьшения (усыхания) надпочеников. Это связано с тем, что надпочечники прекращают или уменьшают продукцию естественных кортикостероидов и этот факт является очень важным для понимания, почему нельзя резко прекращать прием этих препаратов. Первое – прием синтетических гормонов не должно прерываться внезапно, так как для надпочечников необходимо время (до нескольких месяцев) чтобы вновь начать выработку естественного гормона. Внезапное прекращение приема кортикостероидов опасно для жизни, возможно развитие острых сосудистых кризов. Вот почему снижение дозы кортикостероидов должно происходить очень медленно в течение недель, а то и месяцев, так как за этот период надпочечники могут адаптироваться к выработке естественного гормона. Второе, что необходимо учитывать при приеме кортикостероидов – это любое физическое напряжение или эмоциональный стресс, в том числе хирургическая операция, удаление зуба требует дополнителького введения кортикостероидов.
Для пациентов СКВ, у которых вовлечены жизненно-важные органы – это почки или центральная нервная система, или поражение многих органов, могут использоваться лекарственные препараты, называемые иммуносупрессорами. Иммуносупрессоры, такие как, азатиоприн (Имуран) и циклофосфамид (цитоксан), сдерживают сверхактивную иммунную систему, блокируя продукцию одних иммунных клеток и сдерживая действие других. К группе этих препаратов относится и метотрексат (Фолекс, Мексат, Ревматрекс). Эти лекарства могут даваться в виде таблеток или в инфузии (капая лекарство в вену через маленькую трубку). Побочные эффекты могут включать тошноту, рвоту, выпадение волос, проблемы с мочевым пузырем, уменьшение фертильности и увеличение риска рака или инфекции. Риск побочных эффектов увеличивается с длительностью лечения. Как и при других видах лечения волчанки, есть риск рецидива симптомов после отмены иммунносупрессоров, поэтому лечение должно быть длительным и отмена и регуляция дозы требует тщательного врачебного контроля. Больным, получающим терапию иммуносупрессивными препаратами необходимо также тщательно регистрировать дозу этих препаратов в своем дневнике. Пациенты с этими препаратами должны регулярно 1-2 раза в неделю сдавать общий анализ крови и мочи и необходимо помнить, что при присоединении вторичной инфекции или снижении количества клеток крови (лейкоцитов ниже 3 тысячи, тромбоцитов ниже 100 тысячи) прием препарата временно прекращается. Возобновление лечения возможно после нормализации состояния.
Больным, получающим терапию иммуносупрессивными препаратами необходимо также тщательно регистрировать дозу этих препаратов в своем дневнике. Пациенты с этими препаратами должны регулярно 1-2 раза в неделю сдавать общий анализ крови и мочи и необходимо помнить, что при присоединении вторичной инфекции или снижении количества клеток крови (лейкоцитов ниже 3 тысячи, тромбоцитов ниже 100 тысячи) прием препарата временно прекращается. Возобновление лечения возможно после нормализации состояния.
Пациенты СКВ, у кого поражены многие системы органов и часто сопровождается присоединением вторичной инфекции, могут получать кроме кортикостероидов внутривенно иммуглобулин, белок крови, который повышает иммунитет и помогает бороться с инфекцией. Иммуглобулин также может использоваться при остром кровотечении у больных СКВ и с тромбоцитопенией или при присоединении инфекций (сепсиса), или для подготовки пациента с волчанкой к операции. Это позволяет уменьшить дозу необходимых кортикостероидов, когда в подобных состояниях показаны их мегадозы.
Работа пациента в тесном контакте с доктором помогает удостовериться, что лечение подобрано правильно. Так как некоторые лекарства могут вызвать нежелательные эффекты, важно сразу сообщать любые новые симптомы своему лечащему врачу. Также важно не прекращать и не менять лечения без предварительного разговора с доктором.
Из-за типа и стоимости лекарств, используемых для лечения волчанки, их возможных серьезных побочных эффектов и отсутствия излечения, многие пациенты ищут другие пути лечения болезни. Некоторые альтернативные попытки, которые были предложены, включают специальные диеты, пищевые добавки, рыбные масла, мази и кремы, хиропрактическое лечение и гомеопатию. Хоты эти методы могут быть не вредными сами по себе, в данное время нет исследований, показывающих, что они помогают. Некоторые альтернативные или дополнительные подходы могут помочь пациенту справиться или уменьшить некоторый стресс, ассоциированный с хроническим заболеванием. Если доктор чувствует, что попытка может помочь и не будет вредна, она может быть включена в план лечения. Однако, важно не пренебрегать регулярной заботой о здоровье или лечением серьезных симптомов препаратами предписанными доктором.
Однако, важно не пренебрегать регулярной заботой о здоровье или лечением серьезных симптомов препаратами предписанными доктором.
Волчанка и качество жизни.
Несмотря на симптомы волчанки и возможные побочные эффекты лечения, больные могут повсеместно поддерживать высокий уровень жизни. Чтобы справиться с волчанкой, надо понять болезнь и ее воздействие на организм. Учась распознавать и предупреждать признаки обострения СКВ, больной может постараться предотвратить ее обострение или уменьшение ее интенсивности. Многие больные волчанкой испытывают повышенную утомляемость, боль, сыпь, лихорадку, дискомфорт в животе, головную боль или головокружение непосредственно перед обострением заболевания. У некоторых пациентов длительное нахождение на солнце может спровоцировать обострение, поэтому важно распланировать адекватный отдых и проведение времени на воздухе в меньший период инсоляции (действия солнечных лучей). Также важно для пациентов с волчанкой регулярно заботиться о здоровье, несмотря на обращение за помощью только тогда, когда симптомы ухудшаются. Постоянный медицинский контроль и лабораторные анализы позволяют доктору заметить любые изменения, что может помочь предотвратить обострение.
Постоянный медицинский контроль и лабораторные анализы позволяют доктору заметить любые изменения, что может помочь предотвратить обострение.
Признаки обострения заболевания
- Повышенная утомляемость
- Боль в мышцах, суставах
- Сыпь
- Лихорадка
- Дискомфорт в животе
- Головная боль
- Головокружения
- Предотвращение обострения
- Учиться распознавать начальные признаки обострения, но не быть запуганным хроническим заболеванием
- Достигнуть взаимопонимания с доктором
- Определить реальные цели и приоритеты
- Лимитировать время пребывания на солнце
- Добиваться здоровья сбалансированной диетой
- Пытаться лимитировать стресс
- Наметить адекватный отдых и достаточное время
- Умеренные физические упражнения по возможности
План лечения приспосабливается соответственно индивидуальным специфическим нуждам и обстоятельствам. При раннем обнаружении новых симптомов лечение может быть более успешным. Доктор может проконсультировать о таких проблемах, как использование средств защиты от солнца, уменьшение стрессов и важности соблюдения режима, планирования занятий и отдыха, а так же как контроля за рождаемостью и планированием семьи. Так как больные волчанкой более подвержены инфекциям, врач может рекомендовать раннюю вакцинацию от простуды для некоторых пациентов.
Доктор может проконсультировать о таких проблемах, как использование средств защиты от солнца, уменьшение стрессов и важности соблюдения режима, планирования занятий и отдыха, а так же как контроля за рождаемостью и планированием семьи. Так как больные волчанкой более подвержены инфекциям, врач может рекомендовать раннюю вакцинацию от простуды для некоторых пациентов.
Пациенты с волчанкой должны периодически обследоваться, например, проходить гинекологическое и маммологическое обследование. Регулярное санирование ротовой полости поможет избежать потенциально опасных инфекций. Если больной принимает кортикостероиды или антималярийные препараты, должно проводиться ежегодное обследование у окулиста для выявления и лечения проблем с глазами.
Оставаться здоровыми требует дополнительных усилий и помощи, поэтому становится особенно важным развивать стратегию поддержания хорошего самочувствия. Хорошее самочувствие включает повышенное внимание к телу, разуму и душе. Одна из первых целей для хорошего самочувствия для больных волчанкой — это справиться со стрессом приобретения хронического заболевания. Эффективное управление стрессом отличается от человека к человеку. Некоторые попытки, которые могут помочь, включают упражнения, технику расслабления такую как медитация и правильное планирование работы и свободного времени.
Эффективное управление стрессом отличается от человека к человеку. Некоторые попытки, которые могут помочь, включают упражнения, технику расслабления такую как медитация и правильное планирование работы и свободного времени.
Рекомендации для сотрудничества с Вашим доктором
- Найдите доктора, который внимательно будет выслушивать Вас
- Обеспечьте полную и аккуратную медицинскую информацию
- Подготовьте лист Ваших вопросов и пожеланий
- Будьте честными и поделитесь своей точкой зрения по волнующим вопросам с Вашим доктором
- Спросите для выяснения или объяснения своего будущего, если Вас это волнует
- Поговорите с другими медицинскими работниками, заботящихся о Вас (медсестрой, терапевтом, невропотологом)
- Не стесняйтесь обсудить некоторые интимные вопросы с доктором (например: рождаемость, контрацепцию)
- Обсудите любые вопросы изменения лечения или применения специфических методов (фитотерапия, эктрасенсс и т.
 д)
д)
Развитие и укрепление хорошей системы поддержки также очень важно. Система поддержки может включать семью, друзей, медицинских работников, в США к ним относятся общественные организации и так называемыю организацию групп поддержки. Участие в группах поддержки может предоставлять эмоциональную помощь, поддержку чувства собственного достоинства и морали, и помогает развивать или улучшать навыки владения собой. Также может помочь получение дополнительных знаний о своем заболевании. Исследования показали, что пациенты, кто хорошо информированы и активно заботятся о себе, отмечают меньше болей, реже посещают доктора, более самоуверенны и остаются более активными.
Беременность и контрацерция для женщин с волчанкой.
Двадцать лет назад женщинам с волчанкой не рекомендовали беременеть из-за высокого риска обострения заболевания и увеличения вероятности выкидыша. Благодаря исследованиям и заботливому лечению все больше женщин с СКВ могут успешно беременеть. Хотя при этом беременность до сих пор предполагает высокий риск, большинство женщин с волчанкой благополучно вынашивают ребенка до конца беременности. Однако, 20-25% «волчаночных» беременностей заканчивается выкидышем, в сравнении с 10-15% беременностей без заболевания. Важно обсуждать или планировать рождение ребенка до беременности. В идеале, женщина должна не иметь признаков или симптомов волчанки и не принимать лекарства за 6 месяцев до беременности.
Однако, 20-25% «волчаночных» беременностей заканчивается выкидышем, в сравнении с 10-15% беременностей без заболевания. Важно обсуждать или планировать рождение ребенка до беременности. В идеале, женщина должна не иметь признаков или симптомов волчанки и не принимать лекарства за 6 месяцев до беременности.
Некоторые женщины могут испытывать легкие или умеренные обострения во время или после беременности, другие нет. У Беременных женщин с волчанкой, особенно у тех, кто принимает кортикостероиды, более вероятно развитие высокого кровяного давления, диабета, гипергликемии (высокого уровня сахара в крови) и почечных осложнений, поэтому постоянная забота и хорошее питание во время беременности весьма важны. Также целесообразно иметь доступ к отделениям интенсивной терапии для новорожденных во время родов, в случае если ребенок потребует неотложной медицинской помощи. Около 25% (1 из 4) детей от женщин с волчанкой рождаются преждевременно, но не страдают от пороков рождения, а в последующем не отстают в развитии, как в физическом, так и умственном, от своих сверстников. Беременные женщины с СКВ не должны прекращать прием преднизолона, только врач-ревматолог может оценить по клинико-лабораторным параметрам вопрос о дозе этих препаратов.
Беременные женщины с СКВ не должны прекращать прием преднизолона, только врач-ревматолог может оценить по клинико-лабораторным параметрам вопрос о дозе этих препаратов.
Важно учитывать выбор лечения во время беременности. Женщина и ее врач должны взвесить потенциальный риск и извлечь пользу при этом для матери и ребенка. Некоторые лекарства, используемые в лечении волчанки, не должны применяться во время беременности, потому что они могут навредить ребенку или вызвать выкидыш. Женщина с волчанкой, которая становиться беременной, нуждается в тесном сотрудничестве с акушером-гинекологом и врачом-ревматологом. Они могут работать вместе для оценки ее индивидуальных нужд и обстоятельств.
Вероятность выкидыша очень реальна для многих беременных женщин с волчанкой. Исследователи сейчас определили два близко связанных между собой волчаночных аутоантитела: антикардиолипиновые антитела и волчаночный антикоагулянт (вместе называемых антифосфолипидными антителами), которые ассоциированы с риском выкидыша. Более половины всех женщин с СКВ имеют эти антитела, которые могут быть определены по анализам крови. Раннее определение этих антител во время беременности может помочь докторам принять шаги для уменьшения риска выкидыша. Беременные женщины, кто по анализам позитивны по этим антителам и у которых до этого были выкидыши, в основном лечатся аспирином или гепарином (лучше низкомолекулярные гепарины) на протяжении всей беременности. В небольшом проценте случаев, у детей от женщин со специфическими антителами, называемых анти-ро и анти-ла, наблюдаются симптомы волчанки, такие как сыпь или низкое содержание клеток крови. Эти симптомы практически всегда временные и не требуют специфической терапии. Большинство детей с симптомами неонатальной волчанки вообще не нуждаются в лечении.
Более половины всех женщин с СКВ имеют эти антитела, которые могут быть определены по анализам крови. Раннее определение этих антител во время беременности может помочь докторам принять шаги для уменьшения риска выкидыша. Беременные женщины, кто по анализам позитивны по этим антителам и у которых до этого были выкидыши, в основном лечатся аспирином или гепарином (лучше низкомолекулярные гепарины) на протяжении всей беременности. В небольшом проценте случаев, у детей от женщин со специфическими антителами, называемых анти-ро и анти-ла, наблюдаются симптомы волчанки, такие как сыпь или низкое содержание клеток крови. Эти симптомы практически всегда временные и не требуют специфической терапии. Большинство детей с симптомами неонатальной волчанки вообще не нуждаются в лечении.
Даже если в течении обострения заболевания СКВ фертильность (возможность забеременеть) несколько уменьшается, существует риск наступления беременностию Незапланированная беременность в период обострения СКВ может негативно сказаться как на здоровье женщины, отягощая симптомы заболевания, так и создать проблемы с вынашиванием. Наиболее безопасным методом контрацепции для женщин СКВ это использование различных колпачков, диафрагм с контрацептивными гелями. В тоже время некоторые женщины могут использовать контрацептивные лекарственные средства для приема внутрь, однако среди них нежелателен прием тех с превалирующим содержанием эстрогенов. Могут быть применены и внутриматочные спирали, но необходимо помнить — риск развития вторичной инфекции у женщин с СКВ более высок по сравнению со женщиной без этого заболевания.
Наиболее безопасным методом контрацепции для женщин СКВ это использование различных колпачков, диафрагм с контрацептивными гелями. В тоже время некоторые женщины могут использовать контрацептивные лекарственные средства для приема внутрь, однако среди них нежелателен прием тех с превалирующим содержанием эстрогенов. Могут быть применены и внутриматочные спирали, но необходимо помнить — риск развития вторичной инфекции у женщин с СКВ более высок по сравнению со женщиной без этого заболевания.
Физические упражнения и СКВ
Больным СКВ важно продолжить ежедневную утреннюю зарядку. Это легче продолжить когда заболевание имеет неактивную форму или, во время обострения вы стали чувствовать себя лучше. Хотя даже в период обострения возможны некоторые упражнения, не требующие особого физического напряжения, что поможет некоторым образом отвлечься от болезни. Кроме того, раннее начало включения физических упражнений поможет вам преодолеть мышечную слабость. Физиотерапевты должны помочь подобрать индивидуальный комплекс упражнений, который может включать комплекс для дыхательной, сердечно-сосудистой системы. Непродолжительные прогулки с постепенным увеличением времени и дистанции расстояния, после исчезновения лихорадки и острых признаков заболевания, пойдут только на пользу больному не только в укреплении собственного здоровья, но и в преодолении синдрома хронической усталости. Необходимо помнить, больные СКВ нуждаются в сбалансированном отдыхе и физических напряжений. Не пытайтесь одновременно делать много дел. Будьте реалистами. Планируйте на перед, задавая темп себе, включайте большинство трудных мероприятий на время, когда вы будете чувствовать себя лучше.
Непродолжительные прогулки с постепенным увеличением времени и дистанции расстояния, после исчезновения лихорадки и острых признаков заболевания, пойдут только на пользу больному не только в укреплении собственного здоровья, но и в преодолении синдрома хронической усталости. Необходимо помнить, больные СКВ нуждаются в сбалансированном отдыхе и физических напряжений. Не пытайтесь одновременно делать много дел. Будьте реалистами. Планируйте на перед, задавая темп себе, включайте большинство трудных мероприятий на время, когда вы будете чувствовать себя лучше.
Диета
Сбалансированная диета одна из важных частей плана лечения. При активности заболевания, когда у Вас ухудшен аппетит, может быть полезен прием поливитаминов, которые могут быть рекомендованы Вашим доктором. Однако еще раз напоминаем, что чрезмерное увлечение витаминами и физическими упражнениями могут осложнить Ваше заболевание.
По поводу алкоголя для больных СКВ основной совет – воздержание. Алкоголь потенциально вредное воздействие на печень, особенно это вредно при приеме лекарственных препаратов, средикоторых метотрексат, циклосфосфан, азатиоприн.
Алкоголь потенциально вредное воздействие на печень, особенно это вредно при приеме лекарственных препаратов, средикоторых метотрексат, циклосфосфан, азатиоприн.
Солнце и искусственное ультрофиолетовое излучение
Более одной трети больных СКВ слишком чувствительны к солнечным лучам (фоточувствительность). Пребывание на солнце даже в течении короткого промежутка времени (не больше 30 минут) или процедуры с ультрофиолетовым излучением вызывают появление различных высыпаний на кожных покровах у 60-80% больных СКВ. Солнечные лучи могут генерализовать проявления кожного васкулита, вызвать обострение СКВ, с проявлениями лихорадки или вовлечением других жизненно-важных органов – почек, сердца, центральной нервной системы. Степень фоточувствительности может варьировать в зависимости от активности СКВ.
Текущие исследования.
Волчанка является темой многочисленных исследований, так как ученые стараются определить, что вызывает волчанку и как лучше ее лечить. Это заболевание в настоящее время считается моделю аутоиммунных заболеваний. Поэтому понимание многих механизмов болезни при СКВ является ключом к понимание тех иммунных нарушений, которые происходят при многих заболеваниях человека. А это и атеросклероз, и онкологические заболевания, и инфекционные и множество других. Некоторые вопросы, над которыми работают ученые, включают: что точно вызывает волчанку и почему? Почему чаще болеют женщины, чем мужчины? Почему больше случаев волчанки в некоторых расовых и этнических группах? Что нарушается в иммунной системе и почему? Как мы можем корректировать функции иммунной системы при ее нарушениях? Как лечить, чтобы уменьшить или излечить симптомы волчанки?
Это заболевание в настоящее время считается моделю аутоиммунных заболеваний. Поэтому понимание многих механизмов болезни при СКВ является ключом к понимание тех иммунных нарушений, которые происходят при многих заболеваниях человека. А это и атеросклероз, и онкологические заболевания, и инфекционные и множество других. Некоторые вопросы, над которыми работают ученые, включают: что точно вызывает волчанку и почему? Почему чаще болеют женщины, чем мужчины? Почему больше случаев волчанки в некоторых расовых и этнических группах? Что нарушается в иммунной системе и почему? Как мы можем корректировать функции иммунной системы при ее нарушениях? Как лечить, чтобы уменьшить или излечить симптомы волчанки?
Чтобы помочь ответить на эти вопросы, ученые делают все возможное, чтобы лучше изучить это заболевание. Они проводят лабораторные исследования, которые сравнивают различные аспекты иммунной системы больных волчанкой и здоровых людей без волчанки. Также используются специальные породы мышей с нарушениями, такими же, как и при волчанке, чтобы объяснить, как функционирует иммунная система при заболевании и определить возможность новых методов лечения.
Активная область исследований — определение генов, которые играют роль в развитии волчанки. Например, ученые предполагают, что у больных волчанкой есть генетический дефект в клеточном процессе, называемом апоптозом или «програмированной гибелью клетки». Апоптоз позволяет организму безопасно избавляться от поврежденных или потенциально опасных для организма клеток. Если есть проблемы в процессе апоптоза, вредные клетки могут задерживаться и повреждать собственные ткани организма. Например, в мутантной породе мышей, которые развивают волчаночно-подобное заболевание, один из генов, который контролирует апоптоз, называемый Fas геном, дефектен. Когда он замещается нормальным геном, мыши больше не развивают признаки заболевания. Исследователи пытаются выяснить, какую роль вовлеченные в апоптоз гены, могут играть в развитии заболеваний человека.
Изучение генов, контролирующих комплемент, ряд белков крови, которые являются важной частью иммунной системы, — другая активная область исследования при волчанке. Комплемент помогает антителам разрушать чужеродные вещества, которые поражают организм. Если есть снижение комплемента, организм менее способен сражаться или разрушать чужеродные вещества. Если эти вещества не уйдут из организма, иммунная система может стать очень активной и начать производить аутоантитела.
Комплемент помогает антителам разрушать чужеродные вещества, которые поражают организм. Если есть снижение комплемента, организм менее способен сражаться или разрушать чужеродные вещества. Если эти вещества не уйдут из организма, иммунная система может стать очень активной и начать производить аутоантитела.
Также ведутся исследования, направленные на определение генов, которые предрасполагают некоторых людей к более серьезным осложнениям волчанки, таким как заболевания почек. Ученые определили ген, ассоциированный с увеличением риска поражения почек при волчанке у американцев африканского происхождения. Изменения в этом гене поражают способность иммунной системы удалять потенциально вредные иммунные комплексы из организма. Исследователи также достигли определенного прогресса в поиске других генов, которые играют роль при волчанке.
Ученые также изучают и другие факторы, влияющие на восприимчивость человека к волчанке. Например, волчанка более характерна для женщин, чем для мужчин, поэтому некоторые исследователи изучают роль гормонов и других различий между мужчинами и женщинами в причине развития заболевания.
Текущее исследование, проводимое Национальным институтом здоровья в США, акцентируется на безопасности и эффективности применения при волчанке оральных контрацептивов (таблетки, контролирующие рождаемость) и гормональной заместительной терапии. Врачи беспокоятся о здравом смысле прописывания оральных контрацептивов или эстрогензаместительной терапии для женщин с волчанкой, так как широко распространена точка зрения, что эстрогены могут ухудшить заболевание. Однако, недавние малочисленные данные предполагают, что эти лекарства могут быть безопасны для некоторых женщин с волчанкой. Ученые надеются, что это исследование даст выбор для безопасных, эффективных методов контроля рождаемости для молодых женщин с волчанкой и возможность женщинам в постменопаузальном периоде с волчанкой применения эстрогензаместительной терапии.
Одновременно идут работы по поиску более успешного лечения волчанки. Основная цель современных научных исследований – это развитие лечения, которое может эффективно уменьшить использование кортикостероидов. Ученые стараются определить комбинацию лекарств, которая была бы более эффективна, чем попытки лечения одним лекарством. Исследователи также заинтересованы в использовании мужских гормонов, называемых андрогенами, как возможное лечение этого заболевания. Другая цель – это улучшить лечение осложнений волчанки в почках и центральной нервной системе. Например, 20-ти летнее исследование показало, что комбинация циклофосфамида и преднизолона помогает задержать или предотвратить почечную недостаточность, одно из тяжелых осложнений волчанки.
Ученые стараются определить комбинацию лекарств, которая была бы более эффективна, чем попытки лечения одним лекарством. Исследователи также заинтересованы в использовании мужских гормонов, называемых андрогенами, как возможное лечение этого заболевания. Другая цель – это улучшить лечение осложнений волчанки в почках и центральной нервной системе. Например, 20-ти летнее исследование показало, что комбинация циклофосфамида и преднизолона помогает задержать или предотвратить почечную недостаточность, одно из тяжелых осложнений волчанки.
Базируясь на новой информации о процессе болезни, ученые используют новые «биологические агенты» для селективного блока частей иммунной системы. Развитие и тестирование этих новых лекарств, которые базируются на соединение, которое встречается по природе в организме, это интересная и обещающая новая область исследования волчанки. Надеются, что эти лекарства будут не только эффективны, но и будут иметь незначительное число побочных эффектов. Предметом выбора лечения, разрабатываемым в настоящее время, является реконструкция иммунной системы с помощью трансплантации костного мозга. В будущем, генная терапия также будет играть важную роль в лечении волчанки. Однако развитие научных исследований требует и больших материальных затрат.
В будущем, генная терапия также будет играть важную роль в лечении волчанки. Однако развитие научных исследований требует и больших материальных затрат.
Ведение беременности и родов у пациентки с системной красной волчанкой
Ведение беременности и родов у пациентки с системной красной волчанкой
Характерная черта современной медицины — большой объем специфической информации и глубина понимания проблемы врачами различных специальностей. Это делает необходимым условием успешной медицинской практики взаимодействие специалистов различного профиля при лечении многих пациентов. Как пример — совместный интерес акушеров-гинекологов и ревматологов к системной красной волчанке (СКВ), обусловленный тем, что этим заболеванием страдают преимущественно женщины детородного возраста, которые хотели бы иметь детей и при этом предпринимают попытки беременеть. Но наличие серьезного хронического заболевания и необходимость постоянного приема лекарств будущей матерью повышают риск неблагоприятного течения заболевания в период беременности и развития ее осложнений.
Все эти риски можно снизить до минимума, если запланировать наступление беременности на фоне отсутствия или снижения активности СКВ, а также тщательно контролировать активность заболевания во время беременности и после родоразрешения. Эти задачи призвано решить сотрудничество наших врачей ревматологов и акушеров-гинекологов, что находит отражение в «историях борьбы» со счастливым финалом — рождением малышей у женщин, которые еще пару десятков лет назад и мечтать не могли о таком счастье.
Клинический случай. Пациентка И., 32 года, в настоящее время наблюдается врачом-ревматологом с диагнозом СКВ. До достижения возраста 28 лет считала себя абсолютно здоровой. В 2015 г. течение первой беременности осложнилось симтомами преэклампсии с прогрессирующей тромбоцитопений (снижения количества тромбоцитов), что потребовало досрочного родоразрешения.
Через несколько месяцев при обследовании по поводу возможной мочевой инфекции был диагностирован тромбоз нижней полой вены, по поводу чего пациентка велась совместно сосудистыми хирургами НИИ СП им. Н.В. Склифосовского и консультативной гемостазиологической бригады 52-й городской больницы. Как причина данного осложнения была заподозрена и, в дальнейшем, подтверждена генетическая тромбофилия.
Н.В. Склифосовского и консультативной гемостазиологической бригады 52-й городской больницы. Как причина данного осложнения была заподозрена и, в дальнейшем, подтверждена генетическая тромбофилия.
Наследственная тромбофилия — генетически обусловленная предрасположенность к повышенному тромбообразованию. Беременность сопровождается физиологической гиперкоагуляцией, которая представляет собой защитный механизм, препятствующий развитию кровотечений в родах или при угрозе прерывания/прерывании беременности. При наложении этих двух факторов риск тромбозов многократно увеличивается, что может стать причиной множества акушерских осложнений.
Подобранная терапия эффективно купировала тромботическое состояние, но сохранялась тромбоцитопения, никак не укладывающаяся ни в имеющийся диагноз, ни в наблюдаемую клиническую картину.
Пристальное внимание врачей не было напрасным, через некоторое время появились новые симптомы: боли в суставах кистей и стоп, сыпь под воздействием солнечных лучей, продолжало снижаться зрение. После непростого диагностического поиска ревматологами ГКБ № 52 был установлен диагноз СКВ и начато патогенетическое лечение.
После непростого диагностического поиска ревматологами ГКБ № 52 был установлен диагноз СКВ и начато патогенетическое лечение.
Системная красная волчанка (СКВ) — хроническое аутоиммунное заболевание с поражением соединительной ткани и сосудов, при котором организм начинает реагировать на собственные клетки как на чужеродные образованием иммунных комплексов. Запускается воспалительный процесс, затрагивающий многие органы и системы: почки, легкие, сердце, кожу, суставы, глаза, клетки крови.
В октябре 2018г. дополнительные задачи поставила наступившая вторая беременность. Появление дополнительных симптомов потребовало диагностических вмешательств и участия других специалистов, в частности, гематологов и офтальмологов. В результате к родам пациентка пришла с диагнозом: системная красная волчанка хронического течения, низкой степени активности с поражением суставов, кожи, системы крови, глаз, АНФ (-),Ат к ДНК (-). АФС-тромбоз нижней полой вены, ВА (+), Наследственная тромбофилия.
Совместное ведение родов и раннего послеродового периода акушерами и ревматологами с привлечением специалистов по проблемам системы свертывания увенчалось успехом. Послеродовой период протекал без осложнений. На 5-е сутки мама и ребенок выписаны домой. Женщина продолжает наблюдаться у ревматолога амбулаторно.
Пациентку наблюдали:
Врач ревматолог, заведующая отделением ревматологии Загребнева А. И.
Врач ревматолог, заведующая КДО ГКБ № 52 Ткаченко С. Н.
Руководитель гематологической службы ГКБ № 52 Мисюрина Е. Н.
Руководитель выездной реанимационной гематологической бригады ГКБ № 52, главный внештатный специалист трансфузиолог Буланов А..jpg) Ю.
Ю.
Зам.главного врача по акушерству и гинекологии Грабовский В. М.
Заведующая родильным домом ГКБ № 52 Кокая. И. Ю.
Врачи акушеры-гинекологи: Осокин И. П., Ефремов А. Н.
PG / VG в электронных сигаретах связано с повреждением легких в хорошо проведенном эксперименте.
Поскольку чиновники здравоохранения пытаются понять растущее число серьезных заболеваний легких, новое экспериментальное исследование с использованием мышей может дать некоторые подсказки о том, что происходит.
Мэтью Мэдисон и его коллеги опубликовали в журнале Journal of Clinical Investigation «Электронные сигареты нарушают гомеостаз липидов легких и врожденный иммунитет независимо от никотина». Они подвергли мышей воздействию аэрозоля электронных сигарет без никотина и с ним и обнаружили, что аэрозоль изменяет липидный (жировой) баланс в легких таким образом, что снижает способность макрофагов легких бороться с инфекциями и нарушает нормальное производство сурфактантов и химических веществ в легких. которые помогают удерживать воздушные мешки от разрушения.Этот эффект не зависел от никотина, но был связан с пропиленгликолем и растительным глицерином, которые являются основными носителями в электронных сигаретах.
которые помогают удерживать воздушные мешки от разрушения.Этот эффект не зависел от никотина, но был связан с пропиленгликолем и растительным глицерином, которые являются основными носителями в электронных сигаретах.
Статья носит технический характер, но ее стоит прочитать, потому что она указывает на биологические пути, которые могут объяснить эти эффекты. Все органы власти, расследующие эти случаи, а также все, кому небезразличны электронные сигареты, должны прочитать эту газету. Это также добавляет к растущему числу случаев, что электронные сигареты — это не просто сигареты без большого количества вредных веществ, но также имеют свои собственные уникальные токсические эффекты.
Рисунок в конце этого сообщения в блоге, взятый из статьи, показывает множество способов, которыми воздействие PG / VG из электронных сигарет (которые авторы называют ENDS, электронными системами доставки никотина) нарушает нормальную функцию легких.
Для людей, которые не хотят копаться в самой статье, Сара Харрисон написала отличный рассказ в Wired , в котором объясняются результаты в плане английского языка. Как и NBC. Обе истории стоит прочитать.
Как и NBC. Обе истории стоит прочитать.
Хотя никотин, похоже, не вызывает такого эффекта, недавняя статья Роберта Таррана из UNC показала, что электронные сигареты вызывают повышение протеаз легких у людей, которые использовали электронные сигареты, которые были похожи на курильщиков, которые, казалось, зависели от никотина.Эти изменения связаны с ХОБЛ.
Вся эта информация указывает на мысль, что множество случаев, привлекающих внимание, вызвано не только загрязнением электронных сигарет, но, скорее, фундаментальным для самого продукта. Возможно, что некоторые другие элементы конкретных продуктов могут усугубить эти условия, или это может зависеть от интенсивности использования. Я предполагаю, что эти случаи существуют уже давно, но распространенность использования электронных сигарет еще не стала достаточно высокой, чтобы создать достаточно случаев, чтобы органы здравоохранения увидели проблему.
Вот аннотация к статье:
Электронные системы доставки никотина (ЭСДН) или электронные сигареты стали популярным средством развлечения среди подростков и взрослых. Хотя использование ЭСДН часто пропагандируется как более безопасная альтернатива обычным сигаретам, лишь несколько всесторонних исследований оценили долгосрочные эффекты испарения никотина и связанных с ним растворителей, пропиленгликоля (PG) и растительного глицерина (VG). Здесь мы показываем, что по сравнению с воздействием дыма у мышей, получавших пары ENDS в течение 4 месяцев, не развилось легочное воспаление или эмфизема.Однако воздействие ЭСДН, независимо от никотина, изменяло гомеостаз липидов легких в альвеолярных макрофагах и эпителиальных клетках. Комплексные липидомные и структурные анализы легких выявили аберрантные фосфолипиды в альвеолярных макрофагах и повышенное содержание фосфолипидов, связанных с сурфактантами, в дыхательных путях. В дополнение к вызванному ENDS отложению липидов, хроническое воздействие паров ENDS подавляло врожденный иммунитет против вирусных патогенов в резидентных макрофагах. Более того, независимо от никотина, мыши, подвергшиеся воздействию ENDS, инфицированные гриппом, демонстрировали усиленное воспаление легких и повреждение тканей.
Хотя использование ЭСДН часто пропагандируется как более безопасная альтернатива обычным сигаретам, лишь несколько всесторонних исследований оценили долгосрочные эффекты испарения никотина и связанных с ним растворителей, пропиленгликоля (PG) и растительного глицерина (VG). Здесь мы показываем, что по сравнению с воздействием дыма у мышей, получавших пары ENDS в течение 4 месяцев, не развилось легочное воспаление или эмфизема.Однако воздействие ЭСДН, независимо от никотина, изменяло гомеостаз липидов легких в альвеолярных макрофагах и эпителиальных клетках. Комплексные липидомные и структурные анализы легких выявили аберрантные фосфолипиды в альвеолярных макрофагах и повышенное содержание фосфолипидов, связанных с сурфактантами, в дыхательных путях. В дополнение к вызванному ENDS отложению липидов, хроническое воздействие паров ENDS подавляло врожденный иммунитет против вирусных патогенов в резидентных макрофагах. Более того, независимо от никотина, мыши, подвергшиеся воздействию ENDS, инфицированные гриппом, демонстрировали усиленное воспаление легких и повреждение тканей. В совокупности наши результаты показывают, что хроническое курение электронных сигарет аберрантно изменяет физиологию эпителиальных клеток легких и резидентных иммунных клеток и способствует плохой реакции на инфекционный вызов. Примечательно, что изменения в гомеостазе липидов и нарушение иммунитета не зависят от никотина, что требует более обширных исследований растворителей-носителей, используемых в электронных сигаретах.
В совокупности наши результаты показывают, что хроническое курение электронных сигарет аберрантно изменяет физиологию эпителиальных клеток легких и резидентных иммунных клеток и способствует плохой реакции на инфекционный вызов. Примечательно, что изменения в гомеостазе липидов и нарушение иммунитета не зависят от никотина, что требует более обширных исследований растворителей-носителей, используемых в электронных сигаретах.
Полная ссылка
Madison MC, Landers CT, Gu BH, Chang CY, Tung HY, You R, Hong MJ, Baghaei N, Song LZ, Porter P, Putluri N, Salas R, Gilbert BE, Levental I, Campen MJ, Corry DB, Kheradmand Ф.Электронные сигареты нарушают гомеостаз липидов легких и врожденный иммунитет независимо от никотина. J Clin Invest. 2019 4 сентября. Pii: 128531. doi: 10.1172 / JCI128531. [Epub перед печатью]. Он доступен здесь.
Тонкий слой поверхностно-активного вещества легких имеет решающее значение для общей физиологии органа и врожденной иммунной функции. Как альвеолярные клетки типа II, так и альвеолярные макрофаги являются основными подгруппами, которые поддерживают и катаболизируют сурфактант на границе раздела жидкость-воздух.Наше исследование показывает, что воздействие ENDS нарушает как липидные, так и белковые компоненты легочного сурфактанта, увеличивая пулы фосфолипидов в дыхательных путях и снижая экспрессию регуляторных белков сурфактанта SP-A и SP-D. Отложение липидов и нарушение иммунной функции — отличительные особенности альвеолярных макрофагов при хроническом лечении ЭСДН. При вирусной инфекции у мышей, подвергшихся воздействию ENDS, наблюдается повышенная заболеваемость и смертность с чрезмерным поражением легких и воспалением на поздних стадиях инфицирования.Главное, что наблюдаемые в нашей модели опосредованные ЭСДН эффекты не зависят от присутствия никотина.
Как альвеолярные клетки типа II, так и альвеолярные макрофаги являются основными подгруппами, которые поддерживают и катаболизируют сурфактант на границе раздела жидкость-воздух.Наше исследование показывает, что воздействие ENDS нарушает как липидные, так и белковые компоненты легочного сурфактанта, увеличивая пулы фосфолипидов в дыхательных путях и снижая экспрессию регуляторных белков сурфактанта SP-A и SP-D. Отложение липидов и нарушение иммунной функции — отличительные особенности альвеолярных макрофагов при хроническом лечении ЭСДН. При вирусной инфекции у мышей, подвергшихся воздействию ENDS, наблюдается повышенная заболеваемость и смертность с чрезмерным поражением легких и воспалением на поздних стадиях инфицирования.Главное, что наблюдаемые в нашей модели опосредованные ЭСДН эффекты не зависят от присутствия никотина.
Исследование добавляет повреждение легких к вредному воздействию мышьяка
23 августа 2013 г.
Новое исследование подтверждает, что воздействие низких или умеренных количеств мышьяка в питьевой воде может ухудшить функцию легких. Дозы примерно 120 частей на миллиард мышьяка в колодезной воде — примерно в 12 раз превышающую дозу, которая обычно считается безопасной, — вызывали повреждение легких, сопоставимое с десятилетиями курения табака.Курение, особенно среди мужчин, еще больше усугубляет ущерб, связанный с мышьяком.
Дозы примерно 120 частей на миллиард мышьяка в колодезной воде — примерно в 12 раз превышающую дозу, которая обычно считается безопасной, — вызывали повреждение легких, сопоставимое с десятилетиями курения табака.Курение, особенно среди мужчин, еще больше усугубляет ущерб, связанный с мышьяком.
Это первое популяционное исследование, четко продемонстрировавшее значительное нарушение функции легких, в некоторых случаях обширное повреждение легких, связанное с воздействием мышьяка от слабого до умеренного.
«Ограничительные дефекты легких, которые мы наблюдали у тех, кто подвергался воздействию мышьяка из колодезной воды, обычно прогрессируют и необратимы», — сказал старший автор исследования Хабибул Ахсан, доктор медицинских наук, доктор медицинских наук, директор Центра эпидемиологии и профилактики рака. Медицинский университет Чикаго.«Они могут со временем привести к серьезным заболеваниям легких».
Исследование, проведенное в Бангладеш и ранее опубликованное в Интернете в American Journal of Respiratory and Critical Care Medicine, добавляет к растущему списку проблем со здоровьем, связанных с мышьяком, который включает рак кожи, мочевого пузыря и легких, сердечно-сосудистые заболевания, когнитивные нарушения. и преждевременная смерть. Приблизительно 77 миллионов человек — почти половина жителей Бангладеш, восьмой по численности населения страны в мире — живут в районах, где колодцы с грунтовыми водами содержат опасные количества мышьяка.
и преждевременная смерть. Приблизительно 77 миллионов человек — почти половина жителей Бангладеш, восьмой по численности населения страны в мире — живут в районах, где колодцы с грунтовыми водами содержат опасные количества мышьяка.
Меньше известно о воздействии повышенных уровней мышьяка из колодезной воды или пищевых продуктов в других частях мира, включая регионы Мексики и США. Исследователи недавно начали пересматривать продукты, такие как рисовый сироп и яблочный сок, которые содержат больше мышьяка, чем 10 частей на миллиард, которые разрешены в питьевой воде в США.
«Трудно проводить тщательные биомедицинские исследования в таком месте, как Бангладеш, где отсутствует инфраструктура для таких проектов, — сказал Асан, — но за последние 12-15 лет мы научились решать эти проблемы.Теперь у нас есть большой ряд связанных результатов, которые отображают воздействие и иллюстрируют серьезность проблемы ».
« Наши результаты подтверждают растущий интерес к более тщательному изучению проблем воздействия мышьяка в Соединенных Штатах », — добавил он.
Исследование, координируемое Ахсаном и соавтором Фаруке Парвезом, DrPH, из Колумбийского университета, стало следующим шагом в долгосрочном исследовании воздействия мышьяка на здоровье человека (HEALS), долгосрочном проекте в Бангладеш, начатом в 2000 году и расширенном. в 2006 году.
Бангладеш, страна крупных рек и низменных равнин, склонна к частым наводнениям, которые, наряду с недостатками санитарии, исторически загрязняли питьевую воду в стране. Это привело к высокому уровню инфекционных заболеваний и детской смертности. В 1960-е годы более 250 000 детей Бангладеш ежегодно умирали от болезней, передаваемых через воду.
Чтобы защитить этих детей, международные благотворительные организации начали масштабную гуманитарную деятельность по обеспечению чистой питьевой водой.Они установили около 10 миллионов скважин с ручным насосом для забора воды из глубоких подземных слоев.
Почти 20 лет спустя, к началу 1990-х, ученые осознали, что этот благонамеренный план провалился. Хотя подземные воды не имели бактериального загрязнения поверхностных источников, они были загрязнены неорганическим мышьяком, токсичным элементом. По данным Всемирной организации здравоохранения, это было «крупнейшее массовое отравление населения в истории».
Хотя подземные воды не имели бактериального загрязнения поверхностных источников, они были загрязнены неорганическим мышьяком, токсичным элементом. По данным Всемирной организации здравоохранения, это было «крупнейшее массовое отравление населения в истории».
Команда HEALS наблюдает за примерно 20 000 человек в Арайхазаре, районе в центральной части Бангладеш, примерно в 20 милях к востоку от столицы Дакки, с широким диапазоном уровней мышьяка в колодцах с питьевой водой.В период с 2005 по 2010 год исследователи обследовали 950 человек, которые сообщили врачам клиники HEALS о респираторных симптомах, таких как кашель и одышка. Исследователи проверили функцию легких каждого пациента и задокументировали его или ее уровни мышьяка.
Они разделили пациентов на три группы в зависимости от воздействия мышьяка, используя два связанных показателя: сколько мышьяка было в их питьевой воде и сколько в их моче.
Затем местные врачи, обученные пульмонологом Кристофером Олопаде, доктором медицины, из Чикагского университета, тщательно измерили функцию легких каждого пациента с помощью спирометра, уделяя особое внимание двум стандартным легочным тестам: форсированный выдох (FEV1, количество воздуха). человек может изгнать за одну секунду) и форсированная жизненная емкость легких (FVC, общий объем выдыхаемого воздуха после полного наполнения легких).
человек может изгнать за одну секунду) и форсированная жизненная емкость легких (FVC, общий объем выдыхаемого воздуха после полного наполнения легких).
Оба измерения показали, что действие мышьяка зависит от дозы. После того, как они исправили возможные искажающие факторы, исследователи обнаружили, что:
- Треть участников подверглась воздействию минимального уровня мышьяка, менее 19 частей на миллиард в воде. У них не было обнаруживаемой потери функции легких, связанной с мышьяком.
- Одна треть подверглась воздействию питьевой воды с относительно низкой дозой мышьяка, от 19 до 97 частей на миллиард. Их функция легких, измеренная по FEV1 и FVC, немного снизилась, но существенно не отличалась от группы с самым низким уровнем мышьяка в воде.
- Одна треть подверглась воздействию умеренной дозы, более 97 частей на миллиард. Для этой группы обе спирометрические переменные были значительно уменьшены. Их ОФВ1 снизился примерно в три раза по сравнению с теми, кто подвергался воздействию от 19 до 97 частей на миллиард, а их ФЖЕЛ упал примерно в шесть раз.

- Курение увеличивало ущерб. Около 90 процентов мужчин курили.
«Эти результаты ясно демонстрируют значительное нарушение функции легких, связанное с более низкими концентрациями, чем сообщалось ранее», — сказал Ахсан.«Больше всего пострадали люди старшего возраста, худые, менее образованные и склонные к употреблению табака. Многие из этих людей имеют ограниченную избыточную емкость легких. Это существенно изменило их жизнь».
«Это говорит о том, что большая часть населения страны подвержена повышенному риску развития серьезных респираторных заболеваний, включая ХОБЛ, бронхит и интерстициальное заболевание легких в будущем», — заключают авторы.
«Это проблема не только для Южной Азии», — сказал Ахсан.«Около 13 миллионов человек в Соединенных Штатах получают воду из частного колодца, который содержит больше мышьяка, чем разрешено законом. И мы все больше и больше осознаем, что воздействие определенных продуктов питания может быть более серьезной проблемой, чем питьевая вода. , проспективное исследование было проведено в этой стране ».
, проспективное исследование было проведено в этой стране ».
Национальные институты здравоохранения финансировали это исследование. Среди других авторов — Мария Аргос из Чикагского университета; Махбуб Юнус, Рабиул Хасан, Алауддин Ахмед и Тарикул Ислам из Чикагского университета и Проектного офиса по мышьяку Колумбийского университета в Дакке; Весна Славкович и Иосиф Х.Грациано из Колумбийского университета; Ю Чен и Стефани Сегерс из Нью-Йоркского университета; и Махмуд Актер из Национального центра астмы, Дакка.
Краткосрочные и долгосрочные последствия COVID-19 для легких
Как COVID-19 влияет на дыхательную систему в целом: в краткосрочной и долгосрочной перспективе?
COVID-19 может влиять на дыхательную систему по-разному и с разным уровнем тяжести заболевания, в зависимости от иммунной системы человека, возраста и сопутствующих заболеваний.Симптомы могут варьироваться от легких, таких как кашель, одышка и лихорадка, до критического заболевания, включая дыхательную недостаточность, шок и отказ многих органов.
Особенно важно, чтобы у пациентов с основным заболеванием легких определенно могло наблюдаться ухудшение этих состояний из-за контрактуры или воздействия COVID-19. При этом COVID-19 может вызвать общее ухудшение этих состояний, таких как астма, хроническая обструктивная болезнь легких (ХОБЛ), интерстициальная болезнь легких и т. Д.
Каково краткосрочное воздействие COVID-19 на легкие для людей, у которых диагностирован COVID-19, а затем они выздоравливают?По данным Всемирной организации здравоохранения, время восстановления составляет около двух недель при легкой инфекции и от трех до шести недель при тяжелой болезни. Однако это значение варьируется и зависит не только от тяжести заболевания, но и от уже имеющихся у пациента сопутствующих заболеваний.
Несколько исследований, проведенных в США и Италии, показывают, что только 39% из тех, кто был госпитализирован, сообщили о возвращении к исходному состоянию здоровья через 14-21 день после постановки диагноза.
Аналогичным образом, в исследовании 143 пациентов, госпитализированных с COVID-19, только 13% не имели симптомов в среднем через 60 дней после начала заболевания.
Наиболее частыми симптомами были одышка (43%), усталость (53%), боли в суставах и грудной клетке.
Тем не менее, были сообщения о стойком тяжелом течении болезни с неделями лихорадки и пневмонии у пациентов с ослабленным иммунитетом.
При более легкой форме инфекции симптомы могут продолжаться. Недавний опрос показал, что только 65% сообщили о возвращении к исходному состоянию здоровья через 14-21 день после постановки диагноза.Те, кто действительно вернулся к исходному состоянию здоровья, сделали это в среднем через семь дней после постановки диагноза. Симптомы, которые могут сохраняться, включают кашель (43%), усталость (35%) и, в редких случаях, лихорадку и озноб у людей с предшествующей легкой инфекцией.
Какие физиологические изменения в структуре и функции легких вызывают серьезные осложнения? Что конкретно вызывает эти изменения? Основной проблемой COVID-19 является газообмен в альвеолах. Обычно между альвеолярным эпителием (клетки типа 1) и капилляром существует очень плотная связь.COVID-19 заражает клетки AT2, убивает их и наводняет альвеолы. Кроме того, есть данные о микротромбозе, который может блокировать сосудистую сторону.
Обычно между альвеолярным эпителием (клетки типа 1) и капилляром существует очень плотная связь.COVID-19 заражает клетки AT2, убивает их и наводняет альвеолы. Кроме того, есть данные о микротромбозе, который может блокировать сосудистую сторону.
Клинически это может проявляться в нескольких состояниях: тяжелая бронхопневмония, острый респираторный дистресс-синдром (ОРДС) или сепсис.
Пневмония — это воспаление и жидкость в легких, из-за чего трудно дышать. Пациенты могут испытывать одышку, жар и кашель, что может быть продуктивным. Более серьезное воспаление может привести к ОРДС, что может потребовать серьезного лечения, включая использование кислородной терапии, включая механическую вентиляцию легких или даже экстракорпоральную мембранную оксигенацию (ЭКМО), которая представляет собой устройство обходного анастомоза легких, которое насыщает кровь кислородом.Если у пациента развивается этот тяжелый синдром, это может привести к более длительным последствиям для легких, таким как фиброз (рубцевание легких).
Сепсис — это синдром аномального воспаления, который обычно возникает в результате инфекции. Это может привести к тому, что несколько органов не будут работать скоординированно. Этот синдром может потребовать поддержки вышедших из строя органов и, следовательно, оказать длительное влияние на их долгосрочную функциональность.
советов, как сохранить здоровье легких
Иногда мы воспринимаем наши легкие как должное.Они поддерживают нас живыми и здоровыми, и по большей части нам не нужно о них думать. Вот почему так важно уделять первоочередное внимание здоровью легких.
В вашем теле есть естественная система защиты, предназначенная для защиты легких, удерживая грязь и микробы в узде. Но есть несколько важных вещей, которые вы можете сделать, чтобы снизить риск заболевания легких. Вот несколько способов сохранить здоровье легких.
Не кури
Курение сигарет — основная причина рака легких и хронической обструктивной болезни легких (ХОБЛ), включая хронический бронхит и эмфизему. Сигаретный дым может сузить дыхательные пути и затруднить дыхание. Это вызывает хроническое воспаление или отек легких, что может привести к хроническому бронхиту. Со временем сигаретный дым разрушает ткань легких и может вызвать изменения, перерастающие в рак. Если вы курите, бросить курить никогда не поздно. Американская ассоциация легких может помочь, когда вы будете готовы.
Сигаретный дым может сузить дыхательные пути и затруднить дыхание. Это вызывает хроническое воспаление или отек легких, что может привести к хроническому бронхиту. Со временем сигаретный дым разрушает ткань легких и может вызвать изменения, перерастающие в рак. Если вы курите, бросить курить никогда не поздно. Американская ассоциация легких может помочь, когда вы будете готовы.
Избегайте воздействия загрязнителей в помещении, которые могут повредить легкие
Пассивное курение, химические вещества в доме и на рабочем месте, а также радон — все это может вызвать или усугубить заболевание легких.Сделайте свой дом и машину свободными от табачного дыма. Проверьте свой дом на радон. Не выполняйте упражнения на открытом воздухе в дни с плохим воздухом И поговорите со своим врачом, если вы обеспокоены тем, что что-то в вашем доме, школе или на работе может вызвать у вас заболевание.
Сведите к минимуму воздействие загрязнения наружного воздуха
Качество воздуха снаружи может меняться день ото дня и иногда вредно для здоровья дышать. Знание того, как загрязнение атмосферного воздуха влияет на ваше здоровье, и полезные стратегии минимизации длительного воздействия могут помочь вам и вашей семье в благополучии.Изменение климата и стихийные бедствия также могут напрямую влиять на здоровье легких.
Знание того, как загрязнение атмосферного воздуха влияет на ваше здоровье, и полезные стратегии минимизации длительного воздействия могут помочь вам и вашей семье в благополучии.Изменение климата и стихийные бедствия также могут напрямую влиять на здоровье легких.
Предотвратить инфекцию
Простуда или другая респираторная инфекция иногда могут стать очень серьезными. Есть несколько способов защитить себя:
- Часто мойте руки водой с мылом. Чистящие средства на спиртовой основе — хорошая замена, если вы не можете мыться.
- Избегает скопления людей в сезон простуд и гриппа.
- Хорошая гигиена полости рта может защитить вас от микробов во рту, ведущих к инфекциям.Чистите зубы не реже двух раз в день и посещайте стоматолога не реже одного раза в шесть месяцев.
- Делайте ежегодные прививки от гриппа. Поговорите со своим врачом, чтобы узнать, подходит ли вам вакцина от пневмонии.
- Если заболел, держи при себе! Защищайте окружающих вас людей, в том числе своих близких, соблюдая дистанцию.
 Не ходите на работу или в школу дома, пока вам не станет лучше.
Не ходите на работу или в школу дома, пока вам не станет лучше.
Регулярные осмотры
Регулярные осмотры помогают предотвратить заболевания, даже если вы чувствуете себя хорошо.Это особенно верно в отношении заболеваний легких, которые иногда остаются незамеченными, пока не становятся серьезными. Во время осмотра ваш лечащий врач послушает ваше дыхание и выслушает ваши опасения. Если вам нужна медицинская страховка, узнайте больше о возможных вариантах.
Exercise
Если вы молоды или стары, стройны или крупны, здоровы или живете с хроническим заболеванием или инвалидностью, физическая активность может помочь сохранить ваши легкие здоровыми. Узнайте больше о том, как упражнения могут укрепить ваши легкие.
Предупреждающих знаков заболевания легких
Нежный кашель или легкий хрип едва заметны в течение наших загруженных дней, но критически важно обращать внимание даже на легкие симптомы. Иногда люди думают, что проблемы с дыханием — это просто то, что приходит с возрастом. Важно обращать внимание на эти симптомы, поскольку они могут быть первыми признаками заболеваний легких, включая ХОБЛ, астму и рак легких. Знание ранних признаков заболевания легких может помочь вам получить лечение до того, как болезнь станет серьезной или даже опасной для жизни.Если вы заметили какой-либо из следующих предупреждающих знаков, как можно скорее запишитесь на прием к врачу. Раннее обнаружение может спасти вам жизнь.
Важно обращать внимание на эти симптомы, поскольку они могут быть первыми признаками заболеваний легких, включая ХОБЛ, астму и рак легких. Знание ранних признаков заболевания легких может помочь вам получить лечение до того, как болезнь станет серьезной или даже опасной для жизни.Если вы заметили какой-либо из следующих предупреждающих знаков, как можно скорее запишитесь на прием к врачу. Раннее обнаружение может спасти вам жизнь.
Предупреждающие знаки
Хронический кашель: Кашель, который у вас длился восемь недель или дольше, считается хроническим. Это важный ранний симптом, указывающий на то, что с вашей дыхательной системой что-то не так.
Одышка: Не нормально испытывать одышку, которая не проходит после тренировки или которая возникает после небольшой нагрузки или ее отсутствия.Тяжелое или затрудненное дыхание — ощущение, что тяжело дышать — также является предупреждающим знаком.
Хроническое образование слизи: Слизь, также называемая мокротой или мокротой, вырабатывается дыхательными путями в качестве защиты от инфекций или раздражителей. Если слизь вырабатывается месяц или дольше, это может указывать на заболевание легких.
Если слизь вырабатывается месяц или дольше, это может указывать на заболевание легких.
Свистящее дыхание: Шумное дыхание или хрипы — признак того, что что-то необычное блокирует дыхательные пути ваших легких или делает их слишком узкими.
Кашель с кровью: Если вы кашляете кровью, она может исходить из легких или верхних дыхательных путей. Откуда бы он ни исходил, он сигнализирует о проблеме со здоровьем.
Хроническая боль в груди: Необъяснимая боль в груди, которая длится в течение месяца или более, особенно если она усиливается при вдохе или кашле, также является предупреждающим знаком.
Разговор с врачом
Подготовьтесь к посещению вашего поставщика медицинских услуг, выполнив следующие действия:
- Возьмите с собой копию своей медицинской документации.Или посмотрите, может ли ваш предыдущий поставщик медицинских услуг прислать копию. Если вы не можете получить свою медицинскую карту, вы также можете написать краткую заметку о своих проблемах со здоровьем, о том, когда они возникли, и о поставщиках медицинских услуг, которые позаботились о вас.

- Составьте список всех лекарств, которые вы сейчас принимаете. Это означает прописанные и отпускаемые без рецепта лекарства, а также травы и добавки, а также любые нетрадиционные методы, которые вы используете для лечения своего состояния.
- Составьте список всех медицинских работников, к которым вы обращаетесь, с указанием причин, по которым вы их посещаете.
- Составьте список симптомов, которые у вас есть, и отметьте, какие из них беспокоят вас больше всего. Запишите, когда они начали и что вы сделали (если что-то сделали), чтобы улучшить их.
Дыхательная недостаточность | Заболевание легких | Проблемы с легкими
Что такое дыхательная недостаточность?
Дыхательная недостаточность — это состояние, при котором в крови недостаточно кислорода или в ней слишком много углекислого газа. Иногда могут быть обе проблемы.
Когда вы дышите, ваши легкие поглощают кислород.Кислород попадает в вашу кровь, которая переносит его к вашим органам. Ваши органы, такие как сердце и мозг, нуждаются в этой богатой кислородом крови для нормальной работы.
Ваши органы, такие как сердце и мозг, нуждаются в этой богатой кислородом крови для нормальной работы.
Другая часть дыхания — это удаление углекислого газа из крови и его выдох. Слишком много углекислого газа в крови может нанести вред вашим органам.
Что вызывает дыхательную недостаточность?
Условия, влияющие на ваше дыхание, могут вызвать дыхательную недостаточность. Эти состояния могут влиять на мышцы, нервы, кости или ткани, поддерживающие дыхание.Или они могут напрямую повлиять на легкие. Эти условия включают
- Заболевания, поражающие легкие, такие как ХОБЛ (хроническая обструктивная болезнь легких), муковисцидоз, пневмония, тромбоэмболия легочной артерии и COVID-19
- Заболевания, влияющие на нервы и мышцы, контролирующие дыхание, такие как боковой амиотрофический склероз (БАС), мышечная дистрофия, травмы спинного мозга и инсульт.
- Проблемы с позвоночником, например сколиоз (искривление позвоночника). Они могут повлиять на кости и мышцы, используемые для дыхания.

- Повреждение тканей и ребер вокруг легких. Это повреждение может вызвать травма груди.
- Передозировка наркотиками или алкоголем
- Травмы при вдыхании, например, от вдыхания дыма (от огня) или вредных паров
Каковы симптомы дыхательной недостаточности?
Симптомы дыхательной недостаточности зависят от причины и уровня кислорода и углекислого газа в крови.
Низкий уровень кислорода в крови может вызвать одышку и воздушный голод (ощущение, что вы не можете дышать достаточным количеством воздуха).Ваша кожа, губы и ногти также могут иметь голубоватый цвет. Высокий уровень углекислого газа может вызвать учащенное дыхание и спутанность сознания.
Некоторые люди с дыхательной недостаточностью могут стать очень сонными или потерять сознание. У них также может быть аритмия (нерегулярное сердцебиение). Эти симптомы могут возникнуть, если ваш мозг и сердце не получают достаточно кислорода.
Как диагностируется дыхательная недостаточность?
Ваш лечащий врач диагностирует дыхательную недостаточность на основании
.
- Ваша история болезни
- Медицинский осмотр, который часто включает
- Прослушивание легких для выявления ненормальных звуков
- Прислушиваться к своему сердцу для проверки на аритмию
- Ищете синеватый оттенок на коже, губах и ногтях
- Диагностические тесты, например
- Пульсоксиметрия — небольшой датчик, использующий свет для измерения количества кислорода в крови.Датчик идет на кончике пальца или на ухе.
- Анализ газов артериальной крови, тест, который измеряет уровни кислорода и углекислого газа в крови. Образец крови берется из артерии, обычно на запястье.
Как только вам поставят диагноз дыхательной недостаточности, ваш поставщик медицинских услуг будет искать причину ее возникновения. Для этого часто используется рентген грудной клетки. Если ваш поставщик медицинских услуг считает, что у вас может быть аритмия из-за дыхательной недостаточности, вам может быть сделана ЭКГ (электрокардиограмма). Это простой безболезненный тест, который определяет и записывает электрическую активность вашего сердца.
Это простой безболезненный тест, который определяет и записывает электрическую активность вашего сердца.
Какие методы лечения дыхательной недостаточности?
Лечение дыхательной недостаточности зависит от
- Будь то острая (краткосрочная) или хроническая (текущая)
- Насколько это тяжело
- Причина
Острая дыхательная недостаточность может потребовать неотложной медицинской помощи. Возможно, вам понадобится лечение в отделении интенсивной терапии в больнице. Хроническую дыхательную недостаточность часто можно лечить дома.Но если у вас тяжелая хроническая дыхательная недостаточность, вам может потребоваться лечение в центре длительного ухода.
Одна из основных целей лечения — доставить кислород в легкие и другие органы и удалить углекислый газ из организма. Еще одна цель — устранить причину заболевания. Процедуры могут включать
- Кислородная терапия, через назальную канюлю (две маленькие пластиковые трубки, которые входят в ноздри) или через маску, которая надевается на нос и рот
- Трахеостомия, хирургически сделанное отверстие, которое проходит через переднюю часть шеи и попадает в дыхательное горло.
 Дыхательная трубка, также называемая трахеостомией, или трахеостомией, помещается в отверстие, чтобы помочь вам дышать.
Дыхательная трубка, также называемая трахеостомией, или трахеостомией, помещается в отверстие, чтобы помочь вам дышать. - Вентилятор, дыхательный аппарат, который нагнетает воздух в легкие. Он также выводит углекислый газ из ваших легких.
- Другие методы лечения дыхания, , такие как неинвазивная вентиляция с положительным давлением (NPPV), при которой используется умеренное давление воздуха, чтобы ваши дыхательные пути оставались открытыми во время сна. Еще одна процедура — это специальная кровать, которая качается взад и вперед, чтобы помочь вам дышать и выдыхать.
- Жидкости, часто внутривенно (IV), чтобы улучшить кровоток по всему телу. Они также обеспечивают питание.
- Лекарства от дискомфорта
- Лечение причины дыхательной недостаточности. Эти методы лечения могут включать лекарства и процедуры.
Если у вас дыхательная недостаточность, обратитесь к своему врачу для получения постоянной медицинской помощи. Ваш врач может предложить легочную реабилитацию.
Ваш врач может предложить легочную реабилитацию.
Если у вас хроническая дыхательная недостаточность, убедитесь, что вы знаете, когда и где получить помощь при симптомах.Если у вас серьезные симптомы, например проблемы с дыханием или разговором, вам потребуется неотложная помощь. Вам следует позвонить своему врачу, если вы заметили, что ваши симптомы ухудшаются или у вас появились новые признаки и симптомы.
Жизнь с дыхательной недостаточностью может вызывать страх, беспокойство, депрессию и стресс. Разговорная терапия, лекарства и группы поддержки помогут вам почувствовать себя лучше.
NIH: Национальный институт сердца, легких и крови
Исследование добавляет вред легких к вредному воздействию мышьяка — ScienceDaily
Новое исследование подтверждает, что воздействие низких или умеренных количеств мышьяка в питьевой воде может ухудшить функцию легких.Дозы примерно 120 частей на миллиард мышьяка в колодезной воде — примерно в 12 раз превышающую дозу, которая обычно считается безопасной, — вызывали повреждение легких, сопоставимое с десятилетиями курения табака. Курение, особенно среди мужчин, еще больше усугубляет ущерб, связанный с мышьяком.
Курение, особенно среди мужчин, еще больше усугубляет ущерб, связанный с мышьяком.
Это первое популяционное исследование, четко продемонстрировавшее значительное нарушение функции легких, в некоторых случаях обширное повреждение легких, связанное с воздействием мышьяка от слабого до умеренного.
«Ограничительные дефекты легких, которые мы наблюдали у тех, кто подвергался воздействию мышьяка из колодезной воды, обычно прогрессируют и необратимы», — сказал старший автор исследования Хабибул Ахсан, доктор медицинских наук, доктор медицинских наук, директор Центра эпидемиологии и профилактики рака. Медицинский университет Чикаго.«Они могут со временем привести к серьезным заболеваниям легких».
Исследование, проведенное в Бангладеш и ранее опубликованное в Интернете в журнале American Journal of Respiratory and Critical Care Medicine , дополняет растущий список связанных с мышьяком проблем со здоровьем, который включает рак кожи, мочевого пузыря и легких, сердечно-сосудистые заболевания, когнитивные нарушения и преждевременная смерть. Приблизительно 77 миллионов человек — почти половина жителей Бангладеш, восьмой по численности населения страны в мире — живут в районах, где колодцы с грунтовыми водами содержат опасные количества мышьяка.
Приблизительно 77 миллионов человек — почти половина жителей Бангладеш, восьмой по численности населения страны в мире — живут в районах, где колодцы с грунтовыми водами содержат опасные количества мышьяка.
Меньше известно о воздействии повышенных уровней мышьяка из колодезной воды или пищевых продуктов в других частях мира, включая регионы Мексики и США. Исследователи недавно начали пересматривать продукты, такие как рисовый сироп и яблочный сок, которые содержат больше мышьяка, чем 10 частей на миллиард, которые разрешены в питьевой воде в США.
«Трудно проводить тщательные биомедицинские исследования в таком месте, как Бангладеш, где отсутствует инфраструктура для таких проектов, — сказал Асан, — но за последние 12-15 лет мы научились решать эти проблемы.Теперь у нас есть большой ряд связанных результатов, которые отображают подверженность и иллюстрируют серьезность проблемы ».
«Наши результаты подтверждают растущий интерес к более тщательному изучению вопросов воздействия мышьяка в Соединенных Штатах», — добавил он.
Исследование, координируемое Ахсаном и соавтором Фаруке Парвезом, DrPH, из Колумбийского университета, стало следующим шагом в долгосрочном исследовании воздействия мышьяка на здоровье человека (HEALS), долгосрочном проекте в Бангладеш, начатом в 2000 году и расширенном. в 2006 году.
Страна с крупными реками и низменными равнинами, Бангладеш подвержена частым наводнениям, которые, наряду с недостатками санитарии, исторически загрязняли питьевую воду в стране. Это привело к высокому уровню инфекционных заболеваний и детской смертности. В 1960-х годах более 250 000 бангладешских детей ежегодно умирали от болезней, передаваемых через воду.
Чтобы защитить этих детей, международные благотворительные организации начали масштабную гуманитарную деятельность по обеспечению чистой питьевой водой.Они установили около 10 миллионов скважин с ручным насосом для забора воды из глубоких подземных слоев.
Почти 20 лет спустя, к началу 1990-х, ученые осознали, что этот благонамеренный план провалился. Хотя подземные воды не имели бактериального загрязнения поверхностных источников, они были загрязнены неорганическим мышьяком, токсичным элементом. По данным Всемирной организации здравоохранения, это было «крупнейшее массовое отравление населения в истории».
Хотя подземные воды не имели бактериального загрязнения поверхностных источников, они были загрязнены неорганическим мышьяком, токсичным элементом. По данным Всемирной организации здравоохранения, это было «крупнейшее массовое отравление населения в истории».
Команда HEALS наблюдает за примерно 20 000 человек в Арайхазаре, регионе в центральной части Бангладеш, примерно в 20 милях к востоку от столицы Дакки, с широким диапазоном уровней мышьяка в колодцах с питьевой водой.В период с 2005 по 2010 год исследователи обследовали 950 человек, которые сообщили врачам клиники HEALS о респираторных симптомах, таких как кашель и одышка. Исследователи проверили функцию легких каждого пациента и задокументировали его или ее уровни мышьяка.
Они разделили пациентов на три группы в зависимости от воздействия мышьяка, используя два связанных показателя: сколько мышьяка было в их питьевой воде и сколько в их моче.
Затем местные врачи, обученные пульмонологом Кристофером Олопаде, доктором медицины из Чикагского университета, тщательно измерили функцию легких каждого пациента с помощью спирометра, уделяя особое внимание двум стандартным легочным тестам: форсированному выдоху (ОФВ1, количество воздуха в воздухе). человек может изгнать за одну секунду) и форсированной жизненной емкости легких (ФЖЕЛ, общий объем выдыхаемого воздуха после полного наполнения легких).
человек может изгнать за одну секунду) и форсированной жизненной емкости легких (ФЖЕЛ, общий объем выдыхаемого воздуха после полного наполнения легких).
Оба измерения показали, что действие мышьяка зависит от дозы. После того, как они исправили возможные искажающие факторы, исследователи обнаружили, что: • Треть участников подверглась воздействию минимального уровня мышьяка, менее 19 частей на миллиард в воде. У них не было обнаруживаемой потери функции легких, связанной с мышьяком. • Одна треть подверглась воздействию питьевой воды с относительно низкой дозой мышьяка, от 19 до 97 частей на миллиард. Их функция легких, измеренная по FEV1 и FVC, немного снизилась, но существенно не отличалась от группы с самым низким уровнем мышьяка в воде.• Одна треть подверглась воздействию умеренной дозы, более 97 частей на миллиард. Для этой группы обе спирометрические переменные были значительно уменьшены. Их ОФВ1 снизился примерно в три раза по сравнению с теми, кто подвергался воздействию от 19 до 97 частей на миллиард, а их ФЖЕЛ упал примерно в шесть раз. • Курение увеличивало ущерб. Около 90 процентов мужчин курили.
• Курение увеличивало ущерб. Около 90 процентов мужчин курили.
«Эти результаты ясно демонстрируют значительное нарушение функции легких, связанное с более низкими концентрациями, чем сообщалось ранее», — сказал Ахсан.«Больше всего пострадали люди старшего возраста, худые, менее образованные и склонные к употреблению табака. Многие из этих людей имеют ограниченную избыточную емкость легких. Это существенно изменило их жизнь».
«Это говорит о том, что большая часть населения страны подвержена повышенному риску развития серьезных респираторных заболеваний, включая ХОБЛ, бронхит и интерстициальное заболевание легких в будущем», — заключают авторы.
«Это проблема не только для Южной Азии», — сказал Ахсан.«Около 13 миллионов человек в Соединенных Штатах получают воду из частного колодца, который содержит больше мышьяка, чем разрешено законом. И мы все больше и больше осознаем, что воздействие определенных продуктов питания может быть более серьезной проблемой, чем питьевая вода.

 2008; 75: 361–371.
2008; 75: 361–371. 2007; 57: 318–326.
2007; 57: 318–326. , Szekanecz Z., Devenyi K. et al. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. 2005; 44: 656–661.
, Szekanecz Z., Devenyi K. et al. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. 2005; 44: 656–661. д)
д)
 Не ходите на работу или в школу дома, пока вам не станет лучше.
Не ходите на работу или в школу дома, пока вам не станет лучше.
.gif)
 Дыхательная трубка, также называемая трахеостомией, или трахеостомией, помещается в отверстие, чтобы помочь вам дышать.
Дыхательная трубка, также называемая трахеостомией, или трахеостомией, помещается в отверстие, чтобы помочь вам дышать.